
| A、标准状况下,22.4L水中所含的分子数约为6.02×1023 | ||
B、标准状况下,aL的氧气和氮气的混合物中含有的分子数约为
| ||
| C、常温常压下,含NA个O3分子的气体的物质的量小于1 mol | ||
| D、28gCO与16gO2的体积比为1:1 |
| a |
| 22.4 |
| a |
| 22.4 |


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| A、若固体完全溶解,则粉末中不可能有Cu2O |
| B、若固体不能完全溶解,则粉末中肯定有Cu2O |
| C、若固体完全溶解,溶液中再加KSCN,变红,则原粉末仅是Fe2O3 |
| D、若固体不能完全溶解,溶液中再加KSCN,不变红,则原粉末仅是Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
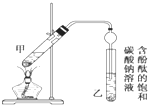 某学生在实验室制取乙酸乙酯的主要步骤如下:
某学生在实验室制取乙酸乙酯的主要步骤如下:| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | x |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:
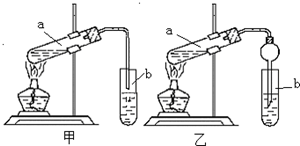 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
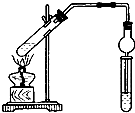 用如图所示实验装置制取乙酸乙酯.回答以下问题:
用如图所示实验装置制取乙酸乙酯.回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
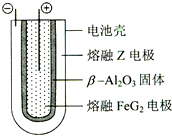 有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:
有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 6 4 2 3 8 |
| B、2 4 3 2 2 6 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、区别苯和乙苯:加酸性高锰酸钾溶液,振荡,观察现象 |
| B、检验无水乙醇中是否含有少量水:加硫酸铜晶体观察现象 |
| C、乙醇的消去反应、皂化反应、淀粉的水解反应均可用浓硫酸作催化剂 |
| D、检验氯代烃中的氯元素时,可先加氢氧化钠溶液加热,再加入硝酸溶液,最后加入硝酸银溶液来进行检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com