
氯化铁是常见的水处理剂。某氯化铁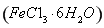 样品含有少量
样品含有少量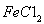 杂质。现要测定其中
杂质。现要测定其中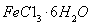 的质量分数,实验按以下步骤进行:
的质量分数,实验按以下步骤进行:
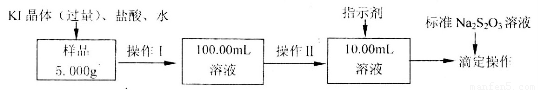
已知有关离子方程式为:
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:_____________________________________。
(2)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、_________(填仪器名称)。
(3)操作II必须用到的仪器是________(选填编号);
a.50mL烧杯???????? b.10mL量筒???????? c.20mL量筒????? d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是__________________________。
(4)滴定时,消耗浓度为0.1000mol/L的标准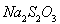 溶液18.00mL。该样品中
溶液18.00mL。该样品中 (式量为270.5)的质量分数为_____________。
(式量为270.5)的质量分数为_____________。
(5)要把样品氯化铁中的少量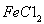 杂质除去,可用的试剂是________(选填编号)。
杂质除去,可用的试剂是________(选填编号)。
a.铁粉????? b.氯水????? c.溴水????? d.双氧水
(6)如果采用以下步骤测定氯化铁样品元素的含量,完成下列填空。
①称量样品? ②加水溶解? ③加足量氨水,沉淀? ④过滤? ⑤灼烧? ⑥称量并进行恒重操作。
还缺少的一步操作是________;在过滤前,需要检验是否沉淀完全,其操作________________________;
判断是否恒重的标准是_______________________________________________________。
(1)Fe3+ + 3H2O  Fe(OH)3 + 3H+ (1分,等号也对,缺反应条件不得分)
Fe(OH)3 + 3H+ (1分,等号也对,缺反应条件不得分)
(2)100ml容量瓶(1分)、胶头滴管(1分)
(3)d(1分) 最后一滴标准液滴入时,锥形瓶中溶液由蓝色变为无色,且半分钟内不变色(1分)
(4)0.9738或97.38% (2分)
(5)bd (2分)
(6)洗涤 (1分)在上层清液中继续滴加氨水,观察有无沉淀产生(1分);连续两次称得的质量相等或不超过0.1g(1分)。
【解析】
试题分析:(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,生成的是氢氧化铁胶体,反应的离子方程式为Fe3+ + 3H2O  Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
(2)因配制一定物质的量浓度的溶液所需要的仪器有:量筒、胶头滴管、烧杯、玻璃棒、一定规格的容量瓶,故还必须有:100mL容量瓶;胶头滴管;
(3)100.00ml的溶液需要精密量具量取,烧杯是粗略量取,量筒只能精确到0.1ml,所以用滴定管精确到0.01ml,选用25mL滴定管量取溶液10.00ml的溶液,故d项正确;碘遇淀粉变蓝色,随标准Na2S2O3溶液滴入和碘单质反应,溶液蓝色变化为无色且半分钟不褪色,说明达到反应终点。
(4)2Fe3++2I-→2Fe2++I2,I2+2S2O32-→2I-+S4O62一,2FeCl3-6H2O~2Fe3+~I2~2S2O32-;滴定时,10.00ml溶液中碘单质消耗浓度为0.1000mol/L的标准Na2S2O3溶液18.17mL,FeCl3?6H2O的物质的量=0.1000mol/L×0.018L=0.0018mol,该样品中100.00ml溶液中所含FeCl3?6H2O的物质的量为0.018mol,质量分数=0.018mol×270.5g/mol÷5.000g×100%=97.38%。
(5)要把样品氯化铁中的少量FeCl2杂质除去,需要加入氧化剂氧化亚铁离子为铁离子,但加入的氧化剂不能引入新的杂质。A、铁粉和铁离子反应,不能和 亚铁离子反应,不符合;
b、氯水可以氧化亚铁离子为铁离子,且不引入新的杂质,符合;c、溴水能氧化亚铁离子,但引入了溴离子,不符合;d、双氧水可以氧化亚铁离子为铁离子,过氧化氢被还原为水,不引入杂质,符合。
(6)实验操作过程分析沉淀需要过滤后洗涤除去表面的杂质;检验是否沉淀完全,可以在上层清液中加入氨水观察是否有沉淀生成;沉淀称量恒重的标准是两次称量质量相同或相差不超过0.001g。
考点:本题考查物质组成和性质的实验验证和实验探究方法,铁及其化合物性质的分析应用,物质除杂,滴定实验测定物质含量的计算应用。


科目:高中化学 来源: 题型:
| ||
| ||
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度/g | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
| 162.5cV |
| m |
| 162.5cV |
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
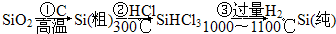
查看答案和解析>>
科目:高中化学 来源:山东省枣庄市2010届高三年级调研考试理综(化学部分)试题 题型:填空题
(11分)
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
①写出步骤①的化学方程式 。
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),提纯SiHCl3的主要化学操作的名称是 ;SiHCl3和SiCl4一样遇水可发生剧烈水解,已知SiHCl3水解会生成两种气态产物,请写出其水解的化学方程式 。
③请写出二氧化硅与氢氟酸反应的化学方程式 。
(2)磁性材料。这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护。最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式 。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
, 。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是 ,三氯化铁溶液可以加速伤口止血,请简述原因 。
(5)高分子材料。可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂
[AlFe(OH)nCl6—n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为 。
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH—CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:山东省枣庄市2010届高三年级调研考试理综(化学部分)试题 题型:填空题
(11分)
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:

①写出步骤①的化学方程式 。
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),提纯SiHCl3的主要化学操作的名称是 ;SiHCl3和SiCl4一样遇水可发生剧烈水解,已知SiHCl3水解会生成两种气态产物,请写出其水解的化学方程式 。
③请写出二氧化硅与氢氟酸反应的化学方程式 。
(2)磁性材料。这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护。最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式 。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
, 。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是 ,三氯化铁溶液可以加速伤口止血,请简述原因 。
(5)高分子材料。可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂
[AlFe(OH)nCl6—n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为 。
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH—CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度/g | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com