
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g)
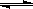 2AB(g)达到化学平衡的标志是
2AB(g)达到化学平衡的标志是
A.容器内的总压强不随时间而变化
B.反应速率v(A2) =v(B2)= 1/2v(AB)
C.单位时间内有n molA2生成的同时就有2n molAB生成
D.容器内混合气体的密度不随时间而变化
科目:高中化学 来源: 题型:阅读理解
 二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012届河北省衡水中学高三下学期二调考试理综试卷(带解析) 题型:填空题
(Ⅰ)氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应。10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为 。
(2)下图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式 。
(3)NH3(g)燃烧的方程式4NH3(g)+7O2(g)==4NO2(g)+6H2O(l),
已知:2H2(g)+O2(g)==2H2O(l) △H=" -483.6" kJ/mol
N2(g)+2O2(g)==2NO2 (g) △H="+67.8" kJ/mol
N2(g)+3H2(g)==2NH3 (g) △H="-92.0" kJ/mol
请计算NH3 (g)的燃烧热 。
| 温度[来源:学§科§网] | 平衡浓度/ (mol L-1)[来源:学*科*网Z*X*X*K] | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |
 2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是 | 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 | | |
 电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
查看答案和解析>>
科目:高中化学 来源:浙江省期中题 题型:单选题
 2AB(g)达到化学平衡的标志是
2AB(g)达到化学平衡的标志是查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省余姚中学高一下学期期中考试理科化学试卷(带解析) 题型:单选题
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g) 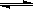 2AB(g)达到化学平衡的标志是
2AB(g)达到化学平衡的标志是
A.容器内的总压强不随时间而变化
B.反应速率v(A2) =v(B2)= 1/2v(AB)
C.单位时间内有n molA2生成的同时就有2n molAB生成
D.容器内混合气体的密度不随时间而变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com