
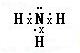
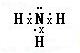
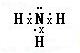 ,故答案为:极性分子,
,故答案为:极性分子,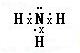 ;
;

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
 (2010?柳州三模)A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图反应关系:
(2010?柳州三模)A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图反应关系:| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:辽宁省沈阳二中2011-2012学年高一上学期12月月考化学试题 题型:022
由前18号元素组成的单质A、B、C(其中A为金属)和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲是电解质.
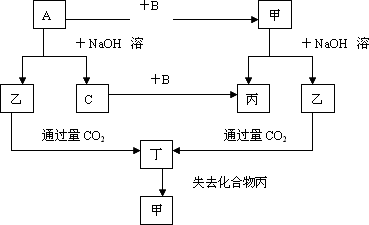
根据以上转化关系回答:
(1)写出下列物质的化学式:
A:________B:________乙:________丁:________
(2)①A与NaOH溶液反应的化学方程式:________.
②乙与过量的CO2反应的离子方程式:________.
查看答案和解析>>
科目:高中化学 来源:广西柳铁一中2010届高三高考模拟冲刺试题(理科综合)化学部分 题型:填空题
(10分) A、B、C、D是由前18号元素组成的四种常见化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如下反应关系:

(1)上述转化过程中包含的反应类型为 。
a置换反应 b化合反应 c分解反应 d复分解反应
(2)乙在甲中燃烧,当有1 mol e-转移,生成液态A时, 放出142.9 kJ的热量,写出该反应的热化学方程式: 。
(3)反应③在一定条件下为可逆反应,经过一段时间该反应达到平衡,写出该反应的化学方程式: 。若将3 mol甲和4 mol C混合充入容积为2 L的密闭容器中,2分钟后,达到平衡。平衡后混合气总物质的量为6 mol,甲的化学反应速率为 。将该平衡混和物缓慢通入水中得到1L溶液,所得溶液物质的量浓度是____________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市重点中学高一(下)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com