

A.(1)在上面元素周期表中画出金属元素与非金属元素的分界线。?
(2)根据NaH的存在,有人提议可将氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可将氢元素放在周期表中的__________族。?
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应显黄色。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应位置。?
②甲元素与硫元素相比较,非金属性较强的是__________(填名称),写出可以验证该结论的一个化学反应方程式__________。
B.
(1)在上面元素周期表中全部是金属元素的区域为__________。?
(a)A (b)B (c)C (d)D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是__________。?
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。?
②甲、乙两元素相比较,金属性较强的是__________(填名称),可以验证该结论的实验是__________。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中?
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应?
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液?
(d)比较这两种元素的气态氢化物的稳定性?
解析:A.本题综合考查元素周期表与元素周期律的相关知识。?
(1)金属与非金属的分界线除ⅠA在氢元素下侧,其他各族元素皆处于周期数主族数的元素的上侧和右侧。?
(2)在周期表中只有第ⅥA的元素的最高正价与最低负价的绝对值相等?
(3)甲元素的核外电子排布为1s22s22p63s23p5,即甲元素为氯;乙元素焰色反应呈黄色,则乙元素为钠元素;而硫、氯处于硫的右侧,比硫的非金属性强,可由反应H2S+Cl2![]() 2HCl + S↓来证明上述结论。?
2HCl + S↓来证明上述结论。?
B.(1)在元素周期表的分区中,只有副族及Ⅷ族的元素全部为金属,故本题的答案为b。?
(2)碳元素形成化合物种类最多的原因,是碳碳之间可形成长链及同分异构现象,即可形成众多的有机物,而绝大部分的有机物都含氢元素,故这种除碳外的短周期元素应为氢元素。
(3)可与冷的浓硫酸作用形成致密的氧化膜的单质为铁和铝,而铁不是短周期元素,故甲为铝,由题意知乙元素的核外电子排布为1s22s22p63s2,即乙为镁元素,镁、铝同周期,镁在铝的左侧,镁的金属性比铝强,从两者与水或酸反应的难易,Mg(OH)2、Al(OH)3的酸碱性强弱比较得之。
答案:A.(1)下表中?

(2)ⅣA?
(3)①下表中

②氯 H2S+Cl2![]() 2HCl + S↓?
2HCl + S↓?
B.(1)b (2)H?
(3)①下表中?
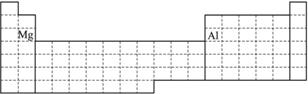
②镁 bc


科目:高中化学 来源: 题型:022
(2005·上海)(A)

(1)在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)根据NaOH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的__________族.
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应呈黄色.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲元素与硫元素相比较,非金属性较强的是________(填名称),写出可以验证该结论的一个化学反应方程式_______.
(B)
(1)在上面元素周期表中全部是金属元素的区域为_______.
|
a.A |
b.B |
c.C |
d.D |
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是______.
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是__________(填名称),可以验证该结论的实验是___________.
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)在上面元素周期表中,全部是金属元素的区域为________________。
A.Ⅰ区 B.Ⅱ区 C.Ⅲ区 D.Ⅳ区
(2)化学性质最不活泼的是__________元素(填元素符号,下同)。
(3)只有负化合价而无正化合价的是__________元素。
(4)最高价氧化物的水化物呈两性的是__________(填化学式),该物质分别与H2SO4、NaOH反应的离子方程式为______________________、______________________。
(5)a、c的最高价氧化物的水化物的碱性_______>__________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(A)

(1)在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)根据NaH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中_______族。
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子(即M层上有7个电子),乙元素的焰色反应呈黄色。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲元素与硫元素相比较,非金属性较强的是______(填名称),写出可以验证该结论的一个化学反应方程式__________。
(B)

(1)在上面元素周期表中全部是金属元素的区域为______。
A.A B.B C.C D.D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是______。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是_____(填名称),可以验证该结论的实验是_____。
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将这两种元素的单质粉末分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源:2014届湖北省武汉市五校高一下学期期中统考化学试卷(解析版) 题型:填空题
(10分)
|
A |
|
|
|||||||||||||||||||||||
|
B |
|
|
|
C |
D |
E |
F |
|
|||||||||||||||||
|
G |
|
H |
|
|
|
I |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
(1)在上面元素周期表中全部是金属元素的区域为___________。
A.a B.b C.c D.d
(2)G元素单质在E元素单质中燃烧时形成的化合物的化学式是______,它是__________(填“共价化合物”或“离子化合物”)。该化合物含有的化学键类型是 ;
该化合物的电子式是 。
(3)表格中九种元素能形成最高价氧化物对应的水化物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是__________,属于两性氢氧化物的是__________。
(4)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 ________(填名称),可以验证该结论的实验是_______。(填编号)
a将在空气中放置已久的这两种元素的块状单质分别放入热水中;
b将这两种元素的单质粉末分别和同浓度的盐酸反应;
c将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液;
d比较这两种元素的气态氢化物的稳定性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com