
室温下,用0.l00mol/L NaOH溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
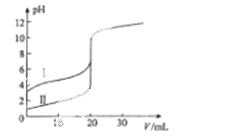
A.II表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH)= 20.00 mL时,两份溶液中c(Cl-)= C(CH3COO-)
D.V(NaOH) =10.00 mL时,醋酸溶液中c(Na+)> C(CH3COO-)> c(H+)> c(OH-)
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,则下列说法正确的是
A.标准状况下,4.48 L水中含有的分子数目为0.2NA
B.0.1 mol钠与足量水反应转移的电子数目为0.1NA
C.0.2 mol·L-1CuSO4溶液中含有的SO42-离子数目为0.2NA
D.0.5molKClO3中含有Cl-的数目为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1CH3COONa溶液与0.1 mol·L-1HCl溶液等体积混合:
c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-)
B.0.1 mol·L-1NH4Cl溶液与0.1 mol·L-1氨水等体积混合(pH>7):
c(NH3·H2O)>c(NH )>c(Cl-)>c(OH-)
)>c(Cl-)>c(OH-)
C.0.1 mol·L-1Na2CO3溶液与0.1 mol·L -1NaHCO3溶液等体积混合:
-1NaHCO3溶液等体积混合:
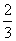 c(Na+)=c(CO
c(Na+)=c(CO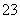 )+c(HCO
)+c(HCO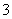 )+c(H2CO3)
)+c(H2CO3)
D.0.1 mol·L-1Na2C2O4溶液与0.1 mol·L-1HCl溶液等体积混合(H2C2O4为二元弱酸):
2c(C2O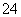 )+c(HC2O
)+c(HC2O )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸是二元中强酸,测得0.01 mol·L-1的草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L-1NaHC2O4溶液中滴加0.01 mol·L-1NaOH溶液,随着NaOH溶液体积的增加,下列说法正确的是 ( )
A.V(NaOH)=0 mL时,c(Na+)>c(H+)>c(HC2O )>c(C2O
)>c(C2O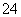 )>c(OH-)
)>c(OH-)
B.V(NaOH)=5 mL时,c(Na+)=c(C2O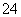 )+c(HC2O
)+c(HC2O )+c(H2C2O4)
)+c(H2C2O4)
C.V(NaOH)=10 mL时,c(Na+)=c(HC2O )+2c(C2O
)+2c(C2O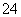 )
)
D.V(NaOH)>10 mL时,c(Na+)>c(C2O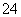 )>c(HC2O
)>c(HC2O )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
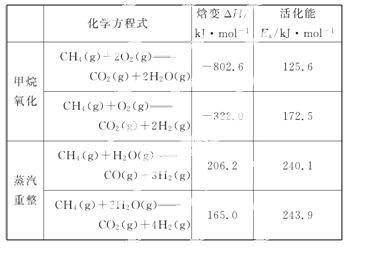
回答下列问题:
(1)反应CO(g)+H2O(g)====CO2(g)+H2(g)的ΔH=_____kJ·mol-1。
(2)在初始阶段,甲烷蒸汽重整的反应速率________甲烷氧化的反应速率(填“大于”“小于”或“等于”)。
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp),则反应CH4(g)+H2O(g)  CO(g)+3H2(g)的Kp=______;随着温度的升高,该平衡常数_________ (填“增大”“减小”或“不变”)。
CO(g)+3H2(g)的Kp=______;随着温度的升高,该平衡常数_________ (填“增大”“减小”或“不变”)。
(4)从能量角度分析,甲烷自热重整方法的先进之处在于___________________________________。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如图:
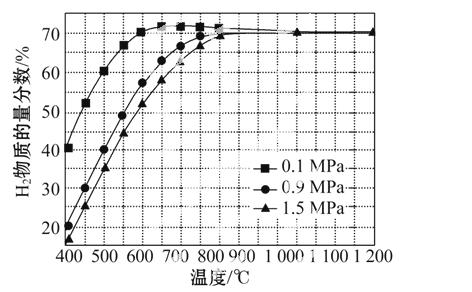
①若要达到H2物质的量分数>65%、CO物质的量分数<10%,以下条件中最合适的是______________。
A.600 ℃,0.9 MPa B.700 ℃,0.9 MPa
C.800 ℃,1.5 MPa D.1 000 ℃,1.5 MPa
②画出600 ℃,0.1 MPa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,10mL0.40mol/L H2O2溶液发生催化分解。不同时刻 测定生成O2的体积(已折算为标准状况)如下表。
测定生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是:
A.氧化铁和稀硫酸反应:Fe2O3+6H+ =2Fe2++3H2O
B.碳酸氢钠溶液中加稀硫酸:CO32-+2H+=H2O+CO2↑
C.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:
Ba2+ + OH- + H+ + SO42- = BaSO4↓+ H2O
D.Cu(OH)2加入H2SO4:2H++Cu(OH)2 = Cu2+ +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl﹣离子完全沉淀.反应中消耗xmolH2SO4、y mol AgNO3.据此得知原混合溶液中的c(Na+)/mol•L﹣1为( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com