
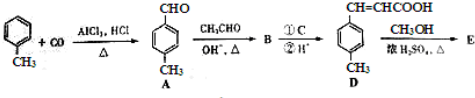
| OH-���� |
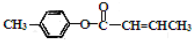 ��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ
��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ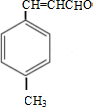 ������-CHO��������������Ϊ-COOH����C=C���ܱ����������ữ�õ�D
������-CHO��������������Ϊ-COOH����C=C���ܱ����������ữ�õ�D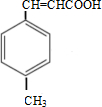 ��D��״�����������Ӧ����EΪ
��D��״�����������Ӧ����EΪ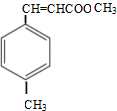 ��Ȼ�����л���Ľṹ�����������
��Ȼ�����л���Ľṹ����������� ������-CHO��������������Ϊ-COOH����C=C���ܱ����������ữ�õ�D
������-CHO��������������Ϊ-COOH����C=C���ܱ����������ữ�õ�D ��D��״�����������Ӧ����EΪ
��D��״�����������Ӧ����EΪ ��
��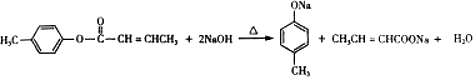 ��
�� ��
��  ��
�� ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ƶ���ɫ��Ӧ����˿���Ȼ�����Һ��ϡ���ᣩ |
| B�������ʵ��������Թܡ�����Ǧ��Һ����������Һ�� |
| C������ͭ������ᾧˮ�����IJⶨ���������¶ȼơ�����ͭ���壩 |
| D����������ȡ�����������������ͣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ʵ������ | ʵ��Ŀ�� |
| A | �����£���pH��ֽ�ֱ�ⶨŨ��Ϊ0.1mol/L NaClO��Һ��0.1mol/L CH3COONa��Һ��pH | �Ƚ�HClO��CH3COOH������ǿ�� |
| B | ���з�̪��Na2CO3��Һ�м�������BaCl2���壬��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| C | ��10mL 0.2mol/L NaOH��Һ�е���2��0.1mol/L MgCl2��Һ��������ɫ�������ٵμ�2��0.1mol/L FeCl3��Һ�������ɺ��ɫ���� | ֤������ͬ�¶��µ� Ksp[Mg��OH��2]��Ksp[Fe��OH��3] |
| D | ����FeCl2��Һʱ���Ƚ�FeCl2��������ϡ����������ˮϡ�ͣ�������Լ�ƿ�м�������ͭ�� | ����Fe2+ˮ�⣬����ֹFe2+������ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SO2��NO2��CO2���������������� |
| B������ͺ�һ�ȼ��鶼�������� |
| C��HC1O��������ʣ�NaClOȴ����ǿ����� |
| D����ˮ��Һ���ܵ����H+�Ļ����ﶼ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��9�� | B��12�� |
| C��15�� | D��18�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
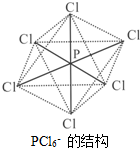 ����������ͬ����Ԫ�أ��㷺��������������ĸ��������У�
����������ͬ����Ԫ�أ��㷺��������������ĸ��������У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
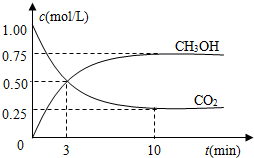 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�| n(CH3OH) |
| n(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ���� | �Լ� | ���� | |
| A | ���� | ��ϩ | ���Ը��������Һ | ϴ�� |
| B | �Ȼ�������Һ | �Ȼ��� | �������� | ���� |
| C | �������� | ������ | ����������Һ | ���� |
| D | �������� | ���� | ����̼������Һ | ���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com