
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )
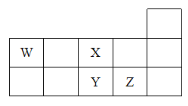
A.Z、Y、W的最高价氧化物的水化物的酸性依次减弱
B.Z、Y、X的原子半径依次减小,非金属性依次减弱
C.气态氢化物的稳定性:H2X>H2Y
D.W的位置是第二周期第ⅣA族
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,按要求回答下列问题:
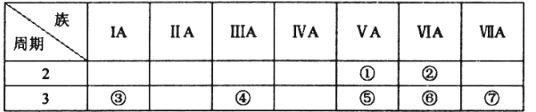
(l)①的简单氢化物的电子式:_________________
(2)⑥的原子结构示意图:________________
(3)⑤、⑥、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序为________________(用化学式表示),③的最高价氧化物对应水化物中含有的化学键的类型为________________
(4)能证明元素⑦比元素⑥的非金属性强的实验事实的是__________ (填字母)
A.常温下元素⑦的单质为气态,而元素⑥的单质为固态
B.元素⑦的气态氢化物比元素⑥的气态氢化物稳定
C.元素⑦的氧化物对应水化物比⑥的氧化物对应水化物酸性强
D.元素⑦的单质能与⑥的氢化物溶液反应生成⑥的单质
(5)④的单质在空气中因表面氧化可以形成致密的氧化物保护膜,从而可以保护内部的单质不被氧化,该氧化物与NaOH溶液反应的离子方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是

A.图甲是常温下用 0.1000 mol·L-1 NaOH 溶液滴定 20.00mL 0.1000 mol·L-1 CH3COOH 的滴定曲线,说明 Q 点表示酸碱中和滴定终点
B.图乙是 1mol X2(g)、1mol Y2(g)反应生成 2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
C.图丙是恒温密闭容器中发生CaCO3(s) CaO(s)+CO2(g)反应时c(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
D.图丁是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照 氯水有O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年7月5日《科学》杂志在线报道:合成一种新的具有超高热导率半导体材料——砷化硼(BAs)。通过反应4BI3(g) + As4(g)![]() 4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是()
4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是()
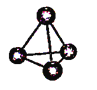
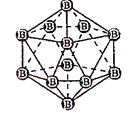
图(a) 图(b) 图(c)
A. 图(a)表示As4结构,As4分子中成键电子对与孤电子对数目之比为3:1
B. 图(b)表示晶态单质硼的B12基本结构单元,该基本单元为正20面体
C. 图(b)所示晶态单质硼的熔点为2180℃,它属于原子晶体
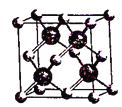
D. 图(c)表示BAs晶胞结构,As原子的配位数为4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构如图所示,有关阿昔洛韦的结构及性质的叙述中正确的是

①1 mol阿昔洛韦在催化剂作用下,最多可与5molH2发生加成反应;②属于芳香烃;③是一种易溶于水的醇;④可以被催化氧化;⑤不能使溴水褪色;⑥可以燃烧;
A. ①②③④⑥B. ②④⑤⑥C. ③④⑤⑥D. ④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li、Na、Mg、C、N、O、S等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_____(填字母)
A.吸收光谱;B.发射光谱。
(2)H2S的VSEPR模型为________,其分子的空间构型为________;结合等电子体的知识判断离子N3–的空间构型为________。
(3)Li2O是离子晶体,其晶格能可通过下图的Born-Haber循环计算得到。

可知Li2O晶格能为______kJ·mol-1。
(4)N、O、Mg元素的前3级电离能如下表所示:

X、Y、Z中为N元素的是______,判断理由是_____________________________。
(5)N5–为平面正五边形,科学家预测将来会制出含N4–、N6–等平面环状结构离子的盐,这一类离子中都存在大π键,可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则N4–离子中的大π键应表示为_________。
),则N4–离子中的大π键应表示为_________。
(6)一种Fe、Si金属间化合物的晶胞结构如下图所示:

晶胞中含铁原子为______个,已知晶胞参数为0.564nm,阿伏伽德罗常数的值为NA,则Fe、Si金属间化合物的密度为___________g·cm–3(列出计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸是生物油的主要成分之一,乙酸制氢具有重要意义:
反应I(热裂解):CH3COOH(g)2CO(g)+2H2(g) △H1
反应II(脱羧基):CH3COOH(g)CH4(g)+CO2(g) △H2
已知:反应I的活化能为(E5-E2)kJ,反应I逆反应的活化能为(E5-E3)kJ,反应II的活化能为(E4-E2)kJ,反应II逆反应的活化能为(E4-E1)kJ,E1到E5能量依次增大
(1)△H1+△H2=___________kJ/mol (用有关E的代数式表示);
(2)在不同温度下,向密闭容器中充入等量醋酸蒸汽,反应相同时间后,测得各气体的产率与温度的关系如图所示:

①约650℃之前,氢气产率低于甲烷的原因是;________________________________;
②约650℃之后,随着温度升高后,氢气产率高于甲烷的原因是:___________;(填编号)
a. 反应II速率减慢
b. 反应I速率加快的程度比反应II大
c. 反应I正向移动,而反应II逆向移动
d. 反应I正向移动的程度大于反应II正向移动的程度
③根据图像分析,该容器中一定发生了另外的副反应,理由是:______________。
(3)投入一定量的乙酸,在相同压强下,经过相同反应时间测得如下实验数据:
温度(℃) | 催化剂 | CH3COOH转化率 | H2的选择性 |
550 | 甲 | 14.5 | 40.2 |
550 | 乙 | 11.1 | 62.1 |
600 | 甲 | 11.2 | 41.2 |
600 | 乙 | 10.3 | 63.3 |
(H2的选择性:转化的CH3COOH中生成H2的百分比)
①表中实验数据表明,在相同温度下不同的催化剂对CH3COOH转化成H2的选择性有显著的影响,其原因是________。
②有利于提高CH3COOH转化为H2平衡转化率的措施有________。
A.使用催化剂甲 B.使用催化剂乙
C.升高反应温度 D.增加反应物的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】邻羟基苯甲酸(俗名水杨酸)其结构简式为如图所示:

(1)水杨酸既可以看成是_______类物质,同时也可以看成_____类物质。
(2)将其与_______溶液作用生成物的化学式为C7H5O3Na,将其与______溶液作用生成物的化学式为C7H4O3Na2。
(3)水杨酸的不同类同分异构体中,属于酚类且也具有苯环的化合物的结构简式为_______,它还可看成是______类物质。
(4)比水杨酸多一个CH2原子团,且与水杨酸属于同系物的取代基数目不同的物质的结构简式为___。
(5)比水杨酸多一个CH2原子团,且与水杨酸不属于同系物的物质的结构简式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com