
| A. | Fe、MnO2 | B. | C、FeS | C. | Si、FeO | D. | CuO、Ag2S |
分析 ①取少量样品加入足量冷的稀硫酸,有气泡产生,固体部分溶解,可知含Fe,与稀硫酸反应生成氢气;
②另取少量样品加入足量浓盐酸并加热,有气泡产生,固体全部溶解,则含二氧化锰,生成气体为氯气,以此来解答.
解答 解:①取少量样品加入足量冷的稀硫酸,有气泡产生,固体部分溶解,可知含Fe,与稀硫酸反应生成氢气;
②另取少量样品加入足量浓盐酸并加热,有气泡产生,固体全部溶解,则含二氧化锰,生成气体为氯气,
而C、Si均与稀硫酸不反应,CuO、Ag2S不能与硫酸反应生成气体,
故选A.
点评 本题考查物质的鉴别与检验,为高频考点,把握物质的性质、发生的反应与现象为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.
如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 推论 |
| A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
| B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
| C | 氨气用于喷泉实验 | 氨气极易溶于水 |
| D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
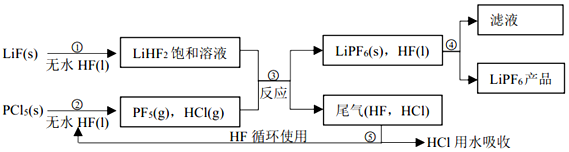
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
| 质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
| 沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉和油脂的水解都是高分子生成小分子的过程 | |
| B. | 2-甲基丙烷和异丁烷互为同系物 | |
| C. |  属于取代反应 属于取代反应 | |
| D. | C3H4Cl2的链状有机物的同分异构体有5种(不考虑立体异构) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com