
| A. | 14C的原子结构示意图 | B. | H2O2的电子式: | ||
| C. | CO2的比例模型: | D. | HClO的结构式:H-O-Cl |
分析 A.元素符号的左上角为质量数,碳为6号元素,碳原子核外有6个电子,根据核外电子排布规律判断;
B.H2O2中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合,无离子存在;
C.比例模型表示原子的相对大小及原子连接顺序、空间结构;
D.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对.
解答 解:A.碳元素质子数为6,电子数为6,原子结构示意图为: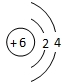 ,故A错误;
,故A错误;
B.H2O2为共价化合物,分子中存在两个氧氢键和一个O-O键,电子式为: ,故B错误;
,故B错误;
C.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,故C错误;
D.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对,次氯酸的电子式为 ,结构式为H-O-Cl,故D正确;
,结构式为H-O-Cl,故D正确;
故选D.
点评 本题考查常用化学用语,题目难度不大,加强基础知识的掌握理解,注意D选项容易受分子式的书写影响.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 16g CH4与18 g NH4+ 所含电子数相等 | |
| B. | 1molNa2O2与足量水反应转移2NA个电子 | |
| C. | 常温下2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CF3Br-1301 | B. | C2F4Cl2-242 | C. | CF2Br2-122 | D. | C2Cl2Br2-2022 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用Cu-Zn-Fe催化剂可大大提高生产效率 | |
| B. | 升高温度,该反应平衡常数K一定增大 | |
| C. | 充入大量CO2气体可提高H2的转化率 | |
| D. | 从平衡混合气体中分离出CH3CH2OH和H2O,可提高CO2和H2的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
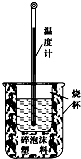 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2SO4溶于水(NH4)2SO4═2NH4++SO42- | |
| B. | H3PO4溶于水H3PO4?3H++PO43- | |
| C. | HF溶于水HF?H++F | |
| D. | NaHS溶于水NaHS═Na++HS-,HS-?H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com