
为了证明长期暴露在空气中的氢氧化钠浓溶液已部分变质,某同学先取2mL试样于试管中,而后进行如下实验,其中不能达到目的是()
| A. | 加入少量盐酸,观察现象 | B. | 加入澄清石灰水,观察现象 | |
| C. | 加入氯化钡溶液,观察现象 | D. | 通适量CO2气体,观察现象 |
| 钠的重要化合物;化学实验方案的评价. | |
| 分析: | 氢氧化钠暴露在空气中,容易和二氧化碳发生反应生成碳酸钠,要证明其变质,证明溶液中含有碳酸钠,即检验碳酸根离子即可. |
| 解答: | 解:A.碳酸钠与少量盐酸反应生成碳酸氢钠,无现象出现,故A选; B.碳酸钠与澄清石灰水反应生成碳酸钙白色沉淀,加入澄清石灰水,若有白色沉淀生成,说明变质,故B不选; C.碳酸钠与氯化钡反应生成碳酸钡白色沉淀,加入氯化钡溶液,若有白色沉淀生成,说明变质,故C不选; D.通适量CO2气体,没有明显现象,不能判断是否变质,故D选; 故选AD. |
| 点评: | 本题考查了氢氧化钠的性质、碳酸根离子的检验,注意检验碳酸根离子时发生化学反应时现象要明显,便于观察. |


科目:高中化学 来源: 题型:
“碘钟”实验中,3I-+S2O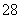 ===I
===I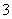 +2SO
+2SO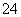 的反应速率可以用I
的反应速率可以用I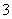 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20 ℃下进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20 ℃下进行实验,得到的数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
回答下列问题:
(1)该实验的目的是_____________________________________________________________。
(2)显色时间t1=________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40 ℃下进行编号③对应浓度的实验,显色时间t2的范围为________(填字母)。
A.<22.0 s B.22.0~44.0 s
C.>44.0 s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
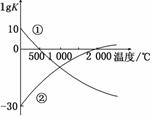
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。
下列说法正确的是( )
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c) v(b)>v(d)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C三种化合物,各取40g相混合,完全反应后,得18g B,49g C,还有D生成.已知D的式量为106.现将22gA和11gB反应,能生成D()
| A. | 1mol | B. | 0.5mol | C. | 0.275mol | D. | 0.25mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
今有H2和CO(体积比为1:2)的混合气体V L,完全燃烧时,所需要同条件O2的体积为()
| A. | 3V L | B. | 2V L | C. | V L | D. | 0.5V L |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将20.0g 14.0%的NaCl溶液跟30.0g 24.0%的NaCl溶液混合,得到密度为1.15g•cm﹣3的混合溶液.
(1)该混合溶液的质量分数为.
(2)该混合溶液的物质的量浓度是3mol•L﹣1
(3)在1000g水中溶解 mol NaCl才能使其浓度与上述混合溶液的浓度相等.
查看答案和解析>>
科目:高中化学 来源: 题型:
国家卫生部在2000年前就决定逐步使用稳定、高效、无毒的二氧化氯取代氯气消毒饮用水.已知二氧化氯溶于水时有亚氯酸根离子(ClO2﹣)生成,且氧化产物与还原产物的物质的量之比为1:1.二氧化氯溶于水的反应方程式2ClO2+H2O═HClO3+HClO2,请标明电子转移方向和数目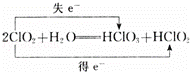 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com