
| 原子 | N | S | O | Si |
| 半径r/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
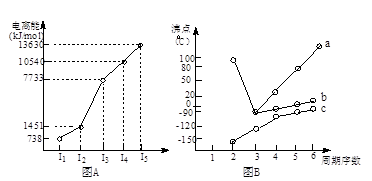
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 | 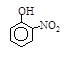 | 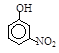 | 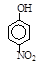 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.基态原子含有未成对电子最多的第二周期元素 |
| B.某激发态为1s22s12p3的原子 |
| C.基态原子最外层电子排布为2s22p6的元素 |
| D.基态原子最外层电子排布为3s23p5的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
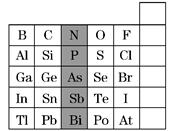
| A.阴影部分元素在周期表中处于第ⅣA族 |
| B.H3AsO4的酸性大于H3PO4 |
| C.根据NaH的存在,也可把氢元素放在第ⅦA族 |
| D.向硅酸钠溶液中加入盐酸可证明氯的非金属性强于硅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.48Ti和50Ti的质子数相同,互称同位素 |
| B.48Ti和50Ti的质量数不同,属于两种元素 |
| C.48Ti和50Ti的质子数相同,是同一种核素 |
| D.48Ti和50Ti的质子数相同,中子数不同,互称同素异形体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.耐高温材料 | B.新型农药材料 | C.半导体材料 | D.新型催化剂材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8、18、32、32 | B.8、18、18、32 |
| C.8、18、18、18 | D.8、8、18、18 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | ② | ③ | | |
| 3 | ④ | | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com