
| A. | X能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,其褪色原理相同 | |
| B. | Y与乙酸反应生成W的反应类型是取代反应 | |
| C. | Z和Y分子中官能团不同 | |
| D. | W的分子式为C4H8O2 |
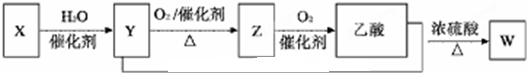
分析 Y氧化生成Z,Z氧化生成乙酸,故Y为CH3CH2OH,Z为CH3CHO,X与水反应得到乙醇,故X为CH2=CH2,乙酸与Y发生酯化反应生成W为CH3COOCH2CH3,据此进行解答.
解答 解:Y氧化生成Z,Z氧化生成乙酸,故Y为CH3CH2OH,Z为CH3CHO,X与水反应得到乙醇,故X为CH2=CH2,乙酸与Y发生酯化反应生成W为CH3COOCH2CH3,
A.X为CH2=CH2,CH2=CH2与溴发生加成反应,使溴的四氯化碳溶液褪色,CH2=CH2与酸性高锰酸钾溶液发生氧化还原反应使其褪色,其褪色原理不相同,故A错误;
B.Y为CH3CH2OH,与乙酸反应生成CH3COOCH2CH3的反应类型是取代反应,故B正确;
C.Z为CH3CHO,含有醛基,Y为CH3CH2OH,含有羟基,二者分子中官能团不同,故C正确;
D.由上述分析可知,W为CH3COOCH2CH3,W的分子式为C4H8O2,故D正确,
故选A.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质及同分异构体等,注意根据X可以连续氧化得到乙酸推断,难度不大.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢键 范德华力 非极性键 | B. | 氢键 氢键 极性键 | ||
| C. | 氢键 极性键 范德华力 | D. | 范德华力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
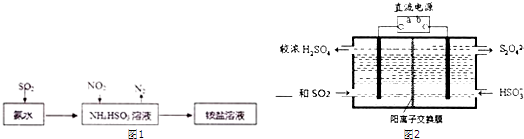
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
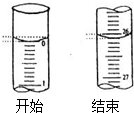 某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 26.01 |
| 第二次 | 20.00 | 1.56 | 30.30 |
| 第三次 | 20.00 | 0.22 | 26.21 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分馏石油时,温度计的水银球必须插入液面以下 | |
| B. | 制备乙酸乙酯时,加料顺序为浓硫酸、乙醇、乙酸 | |
| C. | 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加,直至沉淀刚好溶解为止 | |
| D. | 实验室可用苯和溴水在Fe作催化剂的情况下制备溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
| 4 | ⑩ |
 .元素⑩名称为溴.
.元素⑩名称为溴.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LN2中σ键与π键个数比为1:2 | |
| B. | 反应物和生成物中只有氮气属于非电解质 | |
| C. | 该反应每转移1mol电子,有0.2molKNO3被氧化 | |
| D. | NaN3是只含离子键的离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com