
| A. | 锌粒与稀硫酸的反应 | |
| B. | 甲烷在空气中燃烧的反应 | |
| C. | 灼热的木炭与CO2的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
分析 存在元素的化合价变化的反应为氧化还原反应,常见的吸热反应有:Ba(OH)2•8H2O与NH4Cl反应、大多数的分解反应、C(或氢气)参加的氧化还原反应等,以此来解答.
解答 解:A、金属与水或酸的反应均为氧化还原反应反应,但均为放热反应,故A错误;
B、所有的燃烧均为放热反应,故甲烷在空气中燃烧放热,故B错误;
C、C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO的反应存在化合价的变化,故为氧化还原反应,且为吸热反应,故C正确;
D、Ba(OH)2•8H2O与NH4Cl的反应为复分解反应,故不是氧化还原反应,故D错误.
故选C.
点评 本题考查氧化还原反应,为高考高频考点,侧重反应类型判断的考查,注意化合价角度及归纳常见的吸热反应分析,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铜锌原电池工作时,电子从铜电极流向锌电极 | |
| C. | 氢氧燃料电池可把化学能转化为电能 | |
| D. | 锌锰干电池中,锌电极是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | ①能使溴的四氯化碳溶液褪色,常作植物生长调节剂; ②比例模型如图所示:  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成; ②球棍模型如图所示: 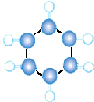 |
| C | ①C、H、O三种元素组成; ②与Na反应产生H2; ③与D反应可生成酯. |
| D | ①C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 | |
| B. | 湿法中FeO42-是氧化产物;干法中O2也是氧化产物 | |
| C. | 干法中每生成1mol Na2FeO4,这个反应共转移4mol电子 | |
| D. | 高铁酸钠中铁显+6价,它在氧化还原反应中通常被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醛基的结构简式为-COH | |
| B. | 乙烯和乙醇都能使溴水和酸性KMnO4溶液褪色 | |
| C. | 乙酸乙酯中的官能团为酯基(-COO-),能发生水解反应 | |
| D. | 苯能与氢气发生加成反应,是因为苯分子中含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
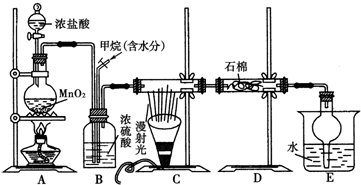 利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如图所示,根据要求填空:
利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如图所示,根据要求填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com