
| A、c1>c2>c3 |
| B、c1>c3>c2 |
| C、c1=c3>c2 |
| D、c1=c2>c3 |
| n |
| V |
| 2V |
| 22.4 |
| 1 |
| 22.4 |
| 4V |
| 22.4 |
| ||
| 5VL |
| 4 |
| 5 |
| 1 |
| 22.4 |
| V |
| 22.4 |
| 1 |
| 22.4 |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
| A、8 | B、16 | C、32 | D、48 |
查看答案和解析>>
科目:高中化学 来源: 题型:
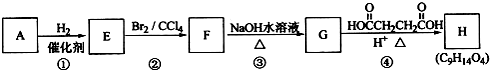
| H+ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| c(SO2)/(mol/L) | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
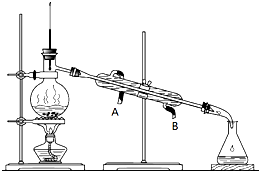 某工厂废液经测定得知主要含有乙醇,其中还有丙酮、乙酸和乙酸乙酯.根据下列各物质的性质
某工厂废液经测定得知主要含有乙醇,其中还有丙酮、乙酸和乙酸乙酯.根据下列各物质的性质| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78.5 | 117.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO42-的空间构型是正四面体形 |
| B、CS2分子中各原子均达8电子稳定结构 |
| C、CH3COOH分子中碳原子的杂化类型有sp2和sp3两种 |
| D、H2O2分子是既含极性键又含非极性键的非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、②③ | C、③④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
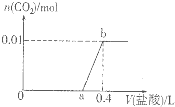 向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )
向NaOH和Na2CO3混合溶液中滴加0.1molgL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示.下列判断正确的是( )| A、在0-a范围内,只发生中和反应 |
| B、ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O |
| C、a=0.2 |
| D、原混合溶液中NaOH与Na2CO3的物质的量之比为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com