
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 单质沸点:W>X>Z | |
| B. | 原子半径:Y>Z>W | |
| C. | Y的氧化物对应的水化物酸性一定比Z的弱 | |
| D. | W、X、Z三种元素组成的化合物一定是共价化合物 |
分析 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.s是元素Y的单质且常温下为淡黄色固体,则s为S,n是元素Z 的单质,Z为Cl,q是元素X的单质,m与r相遇会产生白烟.白烟可能为氯化铵,则m为NH3,r为HCl,n为氯气,q为氮气,X为N元素,结合原子序数可知W为H,X为N,Y为S,Z为Cl,以此来解答.
解答 解:由上述分析可知,W为H,X为N,Y为S,Z为Cl,
A.相对分子质量越大,分子晶体的沸点越大,则单质沸点:Z>X>W,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:Y>Z>W,故B正确;
C.Y的最高价氧化物对应的水化物酸性一定比Z的最高价氧化物对应的水化物酸性弱,HClO为弱酸,不是最高价氧化物对应的水化物,酸性不一定,故C错误;
D.W、X、Z三种元素组成的化合物可能为氯化铵,为离子化合物,故D错误;
故选B
点评 本题考查原子结构与元素周期律,为高频考点,把握物质的性质、相互转化推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性的应用,选项C为解答的易错点,题目难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{4}{5}$ v(NH3)=v(O2) | B. | $\frac{4}{5}$ v(O2)=v(NO) | C. | $\frac{5}{6}$ v(O2)=v(H2O) | D. | $\frac{2}{3}$ v(NH3)=v(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(O2)=0.0125mol/(L•s) | B. | v(NO)=0.06mol/(L•s) | ||
| C. | v(NH3)=0.002mol/(L•s) | D. | v(H2O)=0.0003mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
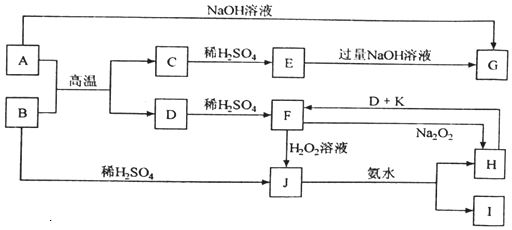
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3(m-n) | B. | m+$\frac{n}{3}$ | C. | $\frac{n-m}{3}$ | D. | $\frac{4n-m}{12}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
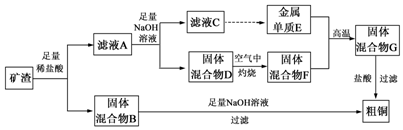
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质 | |
| B. | 氮氧燃料电池常用于肮天飞行器,原因之一是该电池的产物为水,经过处理之后可供宇肮员使用 | |
| C. | 乙醇燃料电池的常用KOH溶液,该电池的负极反应为C2H5OH-12e-+3H2O═CO2↑+12H+ | |
| D. | 甲烷碱性燃料电池工作时OH-定向移动到负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com