
【题目】下列关于HC≡C![]() CH=CHCH3的说法正确的是( )
CH=CHCH3的说法正确的是( )
A.所有碳原子有可能都在同一平面上 B.最多只可能有9个碳原子在同一平面上
C.有7个碳原子可能在同一直线上 D.至少有6个碳原子在同一直线上
【答案】A
【解析】
试题分析:A.双键为平面结构,因此甲基碳原子可在同一平面,三键为直线结构,可在同一平面,苯环可以旋转至和与双键、三键一个平面,故A正确;B.甲基碳原子处于碳碳双键平面内,碳碳三键的直线结构处于苯环的平面内,碳碳双键平面与苯环平面,可以通过碳碳单键的旋转,使2个平面重合,所以最多有11个碳原子共面,故B错误;C.苯环是平面正六边形,两个基团处于苯环的对位位置,碳碳三键为直线结构,连接苯环的碳碳双键的碳原子处于苯中氢原子位置,所以有5个碳原子共线,如图所示5个碳原子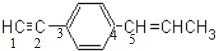 ,故C错误;D.苯环是平面正六边形,两个基团处于苯环的对位位置,碳碳三键为直线结构,连接苯环的碳碳双键的碳原子处于苯中氢原子位置,所以有5个碳原子共线,如图所示5个碳原子
,故C错误;D.苯环是平面正六边形,两个基团处于苯环的对位位置,碳碳三键为直线结构,连接苯环的碳碳双键的碳原子处于苯中氢原子位置,所以有5个碳原子共线,如图所示5个碳原子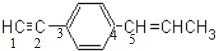 ,故D错误;故选A。
,故D错误;故选A。


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。A组成的单质是最轻的气体;B的原子最外层电子数为次外层的两倍;D为第三周期元素中金属性最强的元素;C和D两种元素核外电子总数之和为19;E元素的最高价氧化物的水化物酸性最强。据此信息,回答下列问题:
(1)写出含有18个中子的E的一种原子符号______,写出A2C的电子式______。
(2)由B和C组成的化合物属于__________化合物(填“离子”或“共价”),该化合物中含有______________(填“离子键”或“共价键”或“离子键和共价键”)。
(3)由B、C、D三种元素组成的化合物,其物质分类属于____(填“酸”或“碱”或“盐”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“ · ”代表一种元素,其中O点代表氢元素.下列说法中错误的是
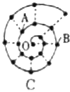
A. 离O点越远的元素原子半径越大
B. 虚线相连的元素处于同一族,A元素位于元素周期表ⅥA族
C. B元素是图中金属性最强的元素
D. B、C最高价氧化物的水化物可以相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50 mL 1.0 mol/LNaCl溶液和50mL,0.5 mol/L CaCl2溶液混合后,若溶液的体积变为二者体积之和,则混合液中Cl-的物质的量浓度为
A. 1 mol /L B. 0.55 mol /L C. 0.67 mol /L D. 2 mol /L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 煤含有苯和甲苯,可干馏后获得苯和甲苯
B. 甲烷、乙烯、NH3和苯在工业上都可通过石油裂解得到
C. 乙醇与乙酸生成乙酸乙酯的反应属于氧化反应
D. 苯和四氯化碳都能萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法不正确的是
A. 分液漏斗和容量瓶在使用前都要检漏
B. 做过碘升华实验的试管可先用酒精清洗,再用水清洗
C. 可用去锈细铁丝或铂丝进行焰色反应实验
D. 红外光谱仪可用来确定物质中含有哪些金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
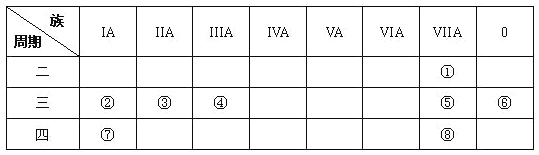
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组气体中,都能用浓硫酸干燥的是( )
A.CO、H2、SO2
B.SO2、H2S、O2
C.HCl、CO2、H2S
D.H2、SO2 、NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于 滴定实验。某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质。

I.制备 Na2S2O3
(1)如图,关闭K1打开K2, 反应开始后,装置c中的产物除 了 Na2S2O3外还有一种无色无味 的气体,这种气体是______。
(2)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1 ,其目的是_______________。待c中溶液冷却后,倒入蒸发皿,通过加热蒸发、冷却结晶和干燥等操作获得Na2S2O3 CH2O晶体。
(3)实验结束后,装置d中的溶质可能有__________________。
探究Na2S2O3的部分化学性质
【分析推理】Na2S2O3可以看成是一个S原子取代了 Na2SO4中一个O原子形成的。据此 推测,下列说法正确的是____________。
A.![]() 和
和![]() 都是正四面体结构 B.
都是正四面体结构 B.![]() 中硫硫键的键长大于硫氧键
中硫硫键的键长大于硫氧键
C.![]() 中的键角均为
中的键角均为![]() D.
D.![]() 中所有原子都满足8电子结构
中所有原子都满足8电子结构
【提出假设】①Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3 溶液pH=7。②从S元素的化合价推测Na2S2O3具有较强的还原性。
【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空):
实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
① | ___________________ | 溶液pH=8 | ___________ |
② | 向新制氯水中滴入适量Na2S2O3溶液 | 氯水褪色 | _____________ |
【实验结论】__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com