
某强酸性溶液X含有Ba 2+ 、Al 3+ 、N 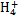 、Fe 2+ 、Fe 3+ 、C
、Fe 2+ 、Fe 3+ 、C 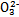 、S
、S 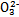 、S
、S 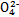 、Cl - 、N
、Cl - 、N 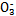 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:
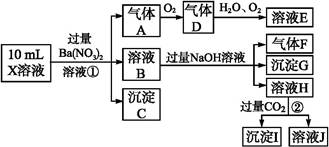
根据以上信息,回答下列问题:
(1)溶液X中除H + 外还肯定含有的离子是 ;不能确定是否含有的离子是 ,若要确定其中阳离子的存在,最可靠的化学方法是 。
(2)沉淀G的化学式为 。
(3)写出有关离子方程式:
步骤①中生成A 。
步骤②生成沉淀I 。
(4)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H + )="0.04" mol,而沉淀C物质的量0.07 mol,能说明(1)中不能确定的阴离子存在的理由是 。
【答案】 (1)Al 3+ 、N
(1)Al 3+ 、N  、Fe 2+ 、S
、Fe 2+ 、S  Cl - 、Fe 3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe 3+ ,若变红则说明含Fe 3+ (没有取样、取量扣分)
Cl - 、Fe 3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe 3+ ,若变红则说明含Fe 3+ (没有取样、取量扣分)
(2)Fe(OH) 3
(3)3Fe 2+ +N 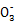 +4H +
+4H +  3Fe 3+ +NO↑+2H 2 O Al
3Fe 3+ +NO↑+2H 2 O Al  +CO 2 +2H 2 O
+CO 2 +2H 2 O  Al(OH) 3 ↓+HC
Al(OH) 3 ↓+HC 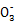
(4)若检验Fe 3+ 肯定存在时,就有Cl - 存在,因为肯定存在的离子电荷总数已相等
【解析】强酸性溶液X一定不含C 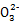 、S
、S 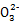 ;在酸性溶液中与Ba(NO 3 ) 2 溶液混合有沉淀C生成,可知X中含有S
;在酸性溶液中与Ba(NO 3 ) 2 溶液混合有沉淀C生成,可知X中含有S  ,一定无Ba 2+ ;生成气体A只能为NO,所以X中含有还原性物质Fe 2+ ,无N
,一定无Ba 2+ ;生成气体A只能为NO,所以X中含有还原性物质Fe 2+ ,无N 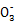 ;溶液B中含有 Fe 3+ ,沉淀G为Fe(OH) 3 ;由气体F可知X中含有N
;溶液B中含有 Fe 3+ ,沉淀G为Fe(OH) 3 ;由气体F可知X中含有N  ,由步骤②可知X中含有Al 3+ ;(4)n(NO)="0.01" mol、n(NH 3 )="0.01" mol、n="0.01" mol、n(H + )="0.04" mol、n(BaSO 4 )="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe 2+ )="3n(NO)=0.03" mol、n(N
,由步骤②可知X中含有Al 3+ ;(4)n(NO)="0.01" mol、n(NH 3 )="0.01" mol、n="0.01" mol、n(H + )="0.04" mol、n(BaSO 4 )="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe 2+ )="3n(NO)=0.03" mol、n(N  )="0.01" mol、n(Al 3+ )="0.01" mol、n(H + )="0.04" mol、n(S
)="0.01" mol、n(Al 3+ )="0.01" mol、n(H + )="0.04" mol、n(S  )="0.07" mol,依据电荷守恒2n(Fe 2+ )+n(N
)="0.07" mol,依据电荷守恒2n(Fe 2+ )+n(N  )+3n(Al 3+ )+n(H + )="0.14" mol=2n(S
)+3n(Al 3+ )+n(H + )="0.14" mol=2n(S  )
)


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
科学家最近发现两种粒子:第一种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子.下列有关这两种粒子的说法不正确的是( )
A. “四中子”不显电性
B. “四中子”的质量数为4,其质量比氢原子大
C. 第二种粒子是氧元素的另一种同位素
D. 第二种粒子的化学式为O4,与O2互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A.H + 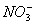 Fe 2+ Na + B.Ag +
Fe 2+ Na + B.Ag + 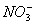 Cl - K +
Cl - K +
C.K + Ba 2+ OH - 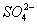 D.Cu 2+
D.Cu 2+ 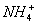 Br - OH -
Br - OH -
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示溶液中发生反应的化学方程式错误的是

| A.MnO 2 +4HCl(浓) MnCl 2 +Cl 2 ↑+2H 2 O |
| B.K 2 Cr 2 O 7 +6FeSO 4 +7H 2 SO 4 =Cr 2 (SO 4 ) 3 +3Fe 2 (SO 4 ) 3 +K 2 SO 4 +7H 2 O |
| C.2Al+2NaOH+2H 2 O=2NaAlO 2 +3H 2 ↑ |
| D.2KMnO 4 +HCOOK+KOH=2K 2 MnO 4 +CO 2 ↑+H 2 O |
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应的实质是__________________________________  ______;元素的化合价降低,发生的是________________反应;氧化还原反应中,还原剂________________电子(填“得”或“失”);试写出Na 2 O 2 与H 2 O反应的化学方程式,并用双线桥标出电子转移的方向和数目:
______;元素的化合价降低,发生的是________________反应;氧化还原反应中,还原剂________________电子(填“得”或“失”);试写出Na 2 O 2 与H 2 O反应的化学方程式,并用双线桥标出电子转移的方向和数目:
____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下图海水综合利用的工业流程图,判断下列说法正确的是
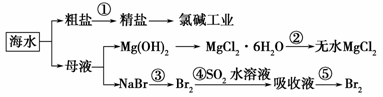
A.除去粗盐中杂质(Mg2+、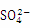 、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
D.从第③步到第⑤步的目的是为了浓缩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com