
ĄŸÌâÄżĄżÒŃÖȘXĄąYĄąZĄąWËÄÖÖÔȘËŰÊÇÔȘËŰÖÜÆÚ±íÖĐÁŹĐűÈęžöȻ͏¶ÌÖÜÆÚ”ÄÔȘËŰŁŹÇÒÔŚÓĐòÊęÒÀŽÎÔöŽóĄŁXĄąWÍŹÖśŚćŁŹYĄąZÎȘÍŹÖÜÆÚ”ÄÏàÁÚÔȘËŰĄŁWÔŚÓ”ÄÖÊŚÓÊę”ÈÓÚYĄąZÔŚÓŚîÍâČă”çŚÓÊęÖźșÍĄŁY”ÄÇ⻯Îï·ÖŚÓÖĐÓĐ3žöčČŒÛŒüĄŁZÔŚÓŚîÍâČă”çŚÓÊęÊÇŽÎÍâČă”çŚÓÊę”Ä3±¶ĄŁÊÔÍÆ¶ÏŁș
Łš1Ł©XĄąYĄąZĄąWËÄÖÖÔȘË۔ķûșĆŁș X________ĄąY__________ĄąZ____________ĄąWĄą________
Łš2Ł©ÓÉÒÔÉÏÔȘËŰÖĐ”ÄÁœÖÖÔȘËŰŚéłÉ”ÄÄÜÈÜÓÚËźÇÒËźÈÜÒșÏÔŒîĐԔĻŻșÏÎï”Ä”çŚÓÊœ·Ö±đÎȘ__________________ŁŹ______________________ĄŁ
Łš3Ł©ÓÉXĄąYĄąZËùĐγɔÄÀëŚÓ»ŻșÏÎïÊÇ________________ŁŹËüÓëW”ÄŚîžßŃő»ŻÎï”ÄËź»ŻÎï”ÄĆšÈÜÒșŒÓÈÈʱ·ŽÓŠ”ÄÀëŚÓ·œłÌÊœÊÇ________________________________________ĄŁ
ĄŸŽđ°žĄżH N O Na ![]()
![]() Ąą
Ąą ![]() NH4NO3 NH4++OH-
NH4NO3 NH4++OH-![]() NH3Ąü+H2O
NH3Ąü+H2O
ĄŸœâÎöĄż
XĄąYĄąZĄąWËÄÖÖÔȘËŰÊÇÔȘËŰÖÜÆÚ±íÖĐÁŹĐűÈęžöȻ͏¶ÌÖÜÆÚ”ÄÔȘËŰŁŹÇÒÔŚÓĐòÊęÒÀŽÎÔöŽóŁŹËùÒÔXÊÇHÔȘËŰŁ»XĄąWÍŹÖśŚćŁŹÔòWÊÇNaÔȘËŰŁ»ZÔŚÓŚîÍâČă”çŚÓÊęÊÇŽÎÍâČă”çŚÓÊę”Ä3±¶ŁŹZÊÇOÔȘËŰĄŁYĄąZÎȘÍŹÖÜÆÚ”ÄÏàÁÚÔȘËŰĄŁWÔŚÓ”ÄÖÊŚÓÊę”ÈÓÚYĄąZÔŚÓŚîÍâČă”çŚÓÊęÖźșÍŁŹÔòYÎȘNÔȘËŰĄŁ
žùŸĘÒÔÉÏ·ÖÎöŁŹŁš1Ł©XĄąYĄąZĄąWËÄÖÖÔȘË۔ķûșĆŁș XÊÇHĄąYÊÇNĄąZÊÇOĄąWÊÇNaĄŁ
Łš2Ł©HĄąNĄąOĄąNaÖĐ”ÄÁœÖÖÔȘËŰŚéłÉ”ÄÄÜÈÜÓÚËźÇÒËźÈÜÒșÏÔŒîĐԔĻŻșÏÎïÊÇ°±ÆűĄąŃő»ŻÄÆĄąčęŃő»ŻÄÆŁŹ”çŚÓÊœ·Ö±đÎȘ![]() ŁŹ
ŁŹ![]() Ąą
Ąą![]() ĄŁ
ĄŁ
Łš3Ł©ÓÉHĄąNĄąOËùĐγɔÄÀëŚÓ»ŻșÏÎïÊÇÏőËáï§ŁšNH4NO3Ł©ŁŹNa”ÄŚîžßŃő»ŻÎï”ÄËź»ŻÎïÊÇNaOHŁŹ NH4NO3ÓëNaOH·ŽÓŠÉúłÉÏőËáÄÆșÍ°±ÆűŁŹÀëŚÓ·œłÌÊœÊÇNH4++OH-![]() NH3Ąü+H2OĄŁ
NH3Ąü+H2OĄŁ


 ÔĶÁżìł”Ï”ÁĐŽđ°ž
ÔĶÁżìł”Ï”ÁĐŽđ°ž
| Äꌶ | žßÖĐżÎłÌ | Äꌶ | łőÖĐżÎłÌ |
| žßÒ» | žßÒ»Ăâ·ŃżÎłÌÍÆŒöŁĄ | łőÒ» | łőÒ»Ăâ·ŃżÎłÌÍÆŒöŁĄ |
| žß¶ț | žß¶țĂâ·ŃżÎłÌÍÆŒöŁĄ | łő¶ț | łő¶țĂâ·ŃżÎłÌÍÆŒöŁĄ |
| žßÈę | žßÈęĂâ·ŃżÎłÌÍÆŒöŁĄ | łőÈę | łőÈęĂâ·ŃżÎłÌÍÆŒöŁĄ |
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄż·ŽÓŠ2SO2(g) + O2(g) ![]() 2SO3(g) ĄśH =-akJ/mol(a>0),ÄÜÁż±ä»ŻÈçÍŒËùÊŸŁŹÏÂÁĐË”·šČ»ŐęÈ·”ÄÊÇ
2SO3(g) ĄśH =-akJ/mol(a>0),ÄÜÁż±ä»ŻÈçÍŒËùÊŸŁŹÏÂÁĐË”·šČ»ŐęÈ·”ÄÊÇ

A. 2SO2(g) +O2(g) ![]() 2SO3(1) ĄśH>-a kJ/mol
2SO3(1) ĄśH>-a kJ/mol
B. čęłÌIIżÉÄÜÊčÓĂÁËŽß»ŻŒÁŁŹÊčÓĂŽß»ŻŒÁČ»żÉÒÔÌážßSO2”ÄÆœșâŚȘ»ŻÂÊ
C. ·ŽÓŠÎï¶ÏŒüÎüÊŐÄÜÁżÖźșÍĐĄÓÚÉúłÉÎïłÉŒüÊÍ·ĆÄÜÁżÖźșÍ
D. œ«2molS02(g)șÍ1 mol 02(g)ÖĂÓÚÒ»ĂܱŐÈĘÆśÖĐłä·Ö·ŽÓŠșó·Ćłö”ÄÈÈÁżĐĄÓÚa kJ
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżșŁÔćÖĐșŹÓĐ·áž»”Ä”âÔȘËŰ(ÒÔI-ĐÎÊœŽæÔÚ)ĄŁÊ”ŃéÊÒÖĐÌáÈĄ”â”ÄÁśłÌÈçÍŒŁș
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() šDĄú
šDĄú![]()
Łš1Ł©Ê”ŃéČÙŚśąÛ”ÄĂûłÆÊÇ__ŁŹËùÓĂÖśÒȘÒÇÆśĂûłÆÎȘ__ĄŁ
Łš2Ł©ÌáÈĄ”â”ÄčęłÌÖĐŁŹżÉč©ŃĄÔń”ÄÓĐ»úÊÔŒÁÊÇ___(Ìî±àșĆ)ĄŁŃĄÔń”ÄÀíÓÉÊÇ___ĄŁ
A.ŸÆŸ«(·Đ”ă78Ąæ) B.ËÄÂÈ»ŻÌŒ(·Đ”ă77Ąæ)
C.žÊÓÍ(·Đ”ă290Ąæ) D.±œ(·Đ”ă80Ąæ)
Łš3Ł©ŽÓ”â”ÄÓĐ»úÈÜÒșÖДÔœ”„ÖÊ”â”Ä·œ·šÊÇ___ĄŁ
Łš4Ł©ČœÖèąÙŚÆÉŐșŁÔćʱŁŹłęĐèÒȘÈęœĆŒÜÍ⣏»čĐèÒȘÓĂ”œ”ÄÊ”ŃéÒÇÆśÊÇ__(ŽÓÏÂÁĐÒÇÆśÖĐŃĄłöËùĐè”ÄÒÇÆśŁŹœ«ŚÖÄžÌîĐŽÔÚżŐ°ŚŽŠ)ĄŁ
A.ÉŐ± B.ÛáÛö C.±íĂæĂó D.ÄàÈęœÇ E.ŸÆŸ«”Æ F.žÉÔïÆś
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżŸÙÊÀÎĆĂû”ÄșîÊÏÖƌ”Äč€ÒŐÁśłÌÈçÏÂÍŒËùÊŸŁŹÏÂÁĐË”·šŐęÈ·”ÄÊÇŁšĄĄĄĄŁ©
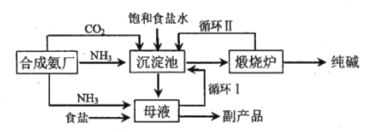
A.ÍùÄžÒșÖĐŒÓÈëÊłŃΔÄÖśÒȘÄż”ÄÊÇÊč![]() žü¶à”ÄÎöłö
žü¶à”ÄÎöłö
B.ŽÓÄžÒșÖĐŸčęŃ»·ąńœűÈëłÁ”íłŰ”ÄÖśÒȘÊÇ![]() Ąą
Ąą![]() șÍ°±Ëź
șÍ°±Ëź
C.łÁ”íłŰÖĐ·ŽÓŠ”Ä»ŻŃ§·œłÌÊœŁș![]()
D.ÉèŒÆŃ»·ąò”ÄÄż”ÄÊÇÊčÔÁÏÂÈ»ŻÄÆ”ÄÀûÓĂÂÊŽóŽóÌáÉę
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżÏÂÁĐ±ÈœÏÖĐŐęÈ·”ÄÊÇ
A. ÏàÍŹĆš¶È”ÄÈęÖÖÈÜÒșŁșąÙ(NH4)2CO3ÈÜÒșĄąąÚNH4HCO3ÈÜÒșĄąąÛNH4NO3ÈÜÒșÖĐ c(NH4+)ŁșąÛ>ąÙ>ąÚ
B. ÏàÍŹpH”ÄÈÜÒșŁșąÙNaClOÈÜÒșĄąąÚNaHCO3ÈÜÒșĄąąÛCH3COONaÈÜÒșÖĐ c(Na+)ŁșąÛ>ąÚ>ąÙ
C. ÍŹĆš¶ÈĄąÍŹÌć»ę”ÄÈÜÒșŁșąÙCH3COONaÈÜÒșĄąąÚNH4ClÈÜÒșĄąąÛNaNO3ÈÜÒșÖĐ pHŁșąÚ>ąÛ>ąÙ
D. ÏàÍŹĆš¶È”ÄÈÜÒșŁșąÙ°±ËźĄąąÚNaOHÈÜÒșĄąąÛBa(OH)2ÈÜÒș c(H+)ŁșąÚ>ąÙ>ąÛ
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżIŁź25ĄæʱŁŹÍù25mLÇâŃő»ŻÄÆ±êŚŒÈÜÒșÖĐÖđ”ÎŒÓÈë0.2 molĄ€LŁ1”ÄÒ»ÔȘËáHAÈÜÒșŁŹpH±ä»ŻÇúÏßÈçÏÂÍŒËùÊŸŁș
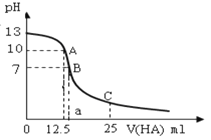
Łš1Ł©žĂÇâŃő»ŻÄÆÈÜÒș”ÄÎïÖÊ”ÄÁżĆš¶ÈÎȘ________molĄ€LŁ1ĄŁ
Łš2Ł©A”ă¶ÔÓŠËá”ÄÌć»ęÎȘ12.5mLŁŹÔòËù”Ă»ìșÏÈÜÒșÖĐÓÉËź”çÀëłö”Äc(OHŁ)Łœ_______ molĄ€LŁ1ĄŁ
Łš3Ł©NaA”ÄËźÈÜÒșÏÔ______ĐÔŁšŃĄÌËᥱĄąĄ°ŒîĄ±Ł©ŁŹÔÒòÊÇŁș________ŁšÓĂÀëŚÓ·œłÌÊœ±íÊŸŁ©ĄŁ
Łš4Ł©ÔÚB”ăËù”Ă»ìșÏÈÜÒșÖĐŁŹc(NaŁ«) Ąąc(AŁ)Ąąc(HŁ«)Ąąc(OHŁ)ÓÉŽó”œĐĄ”ÄËłĐòÊÇ_________ĄŁ
ąòŁźÔÚ25 Ąæ”ÄÌőŒțÏÂŁŹÄłĐ©ÈőËá”Ä”çÀëÆœșⳣÊꥣ
»ŻŃ§Êœ | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | KaŁœ1.8ĄÁ10Ł5 | KaŁœ3.0ĄÁ10Ł8 | Ka1Łœ4.1ĄÁ10Ł7 Ka2Łœ5.6ĄÁ10Ł11 | Ka1Łœ5.9ĄÁ10Ł2 Ka2Łœ6.4ĄÁ10Ł5 |
Łš1Ł©ÎÂ¶ÈĄąĆš¶ÈÏàÍŹ”ÄCH3COOHșÍHClOÈÜÒșŁŹËź”Ä”çÀëłÌ¶ÈÇ°Őß________ șóŐߣšÌ>Ą±Ą°=Ą±»òĄ°<Ą±Ł©ĄŁ
Łš2Ł©Ïà͏ζÈÏÂŁŹpHÏàÍŹ”ÄNaClOșÍCH3COOKÁœÖÖÈÜÒșÖĐŁŹc(CH3COOK)________c(NaClO) ŁšÌ>Ą±Ą°=Ą±»òĄ°<Ą±Ł©ŁŹ[c(NaŁ«)Łc(ClOŁ)]_______[c(KŁ«)Łc(CH3COOŁ)]ŁšÌ>Ą±Ą°=Ą±»òĄ°<Ą±Ł©ĄŁ
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżÈçÍŒËùÊŸŁŹÄłÍŹŃ§ÉèŒÆÒ»žöÈŒÁÏ”çłŰČąÌœŸżÂÈŒîč€Ò”ÔÀíșÍŽÖ͔ğ«Á¶ÔÀíŁŹÆäÖĐÒÒŚ°ÖĂÖĐXÎȘŃôÀëŚÓœ»»»Ä€ĄŁ

žùŸĘÒȘÇó»ŰŽđÏàčŰÎÊÌâŁș
Łš1Ł©ÍšÈëÇâÆű”Ĕ猫ÎȘ___ŁšÌŐęŒ«Ą±»òĄ°žșŒ«Ą±Ł©ŁŹŐęŒ«”Ĕ猫·ŽÓŠÊœÎȘ__ĄŁ
Łš2Ł©ÊŻÄ«”猫(C)”猫ÎȘ___ŁšÌŃôŒ«Ą±»òĄ°ÒőŒ«Ą±Ł©ŁŹFe”猫”Ĕ猫·ŽÓŠÊœÎȘ__ĄŁ
Łš3Ł©·ŽÓŠÒ»¶ÎʱŒäșóŁŹÒÒŚ°ÖĂÖĐÉúłÉÇâŃő»ŻÄÆÖśÒȘÔÚ__ÇűĄŁŁšÌÌúŒ«Ą±»òĄ°ÊŻÄ«Œ«Ą±Ł©
Łš4Ł©ÈçčûŽÖÍÖĐșŹÓĐĐżĄąÒű”ÈÔÓÖÊŁŹÔò±ûŚ°ÖĂÖĐ·ŽÓŠÒ»¶ÎʱŒäșóŁŹÁòËáÍÈÜÒșĆš¶Èœ«__ŁšÌÔöŽóĄ±Ą°ŒőĐĄĄ±»òĄ°Č»±äĄ±Ł©ĄŁ
Łš5Ł©ÈôÔÚ±êŚŒŚŽżöÏÂŁŹÓĐ4.48LŃőÆűČΌӷŽÓŠŁŹÔòÒÒŚ°ÖĂÖĐÌú”猫ÉÏÉúłÉ”ÄÆűÌć”Ä·ÖŚÓÊęÎȘ__Ł»±ûŚ°ÖĂÖĐÒőŒ«ÎöłöÍ”ÄÖÊÁżÎȘ__ĄŁ
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżÏÂÁĐ·ÖŚÓ»òÀëŚÓÖĐŁŹVSEPRÄŁĐÍĂûłÆÓë·ÖŚÓ»òÀëŚÓ”ÄÁąÌćččĐÍĂûłÆČ»Ò»Ö”ÄÊÇ
A. CO2 B. H2O C. CO32© D. CCl4
Č鿎Žđ°žșÍœâÎö>>
żÆÄżŁșžßÖĐ»ŻŃ§ ÀŽÔŽŁș ÌâĐÍŁș
ĄŸÌâÄżĄżËÄÇâß»à«ÊÇłŁÓĂ”ÄÓĐ»úÈÜŒÁŁŹżÉÓÉÓĐ»úÎïAŁš·ÖŚÓÊœŁșC4H8OŁ©ÍščęÏÂÁĐ·ÏßÖÆ”Ă

ÒŃÖȘŁșR1X + R2OH![]() R1OR2 + HX
R1OR2 + HX
ÏÂÁĐË”·šČ»ŐęÈ·”ÄÊÇ
A. CÖĐșŹÓĐ”ÄčÙÄÜÍĆœöÎȘĂŃŒü B. A”ÄœáččŒòÊœÊÇCH3CH=CHCH2OH
C. DșÍEŸùÄÜÊčËáĐÔžßĂÌËáŒŰÈÜÒșÍÊÉ« D. ąÙąÛ”Ä·ŽÓŠÀàĐÍ·Ö±đÎȘŒÓłÉ·ŽÓŠĄąÏûÈ„·ŽÓŠ
Č鿎Žđ°žșÍœâÎö>>
°Ù¶ÈÖÂĐĆ - Á·Ï°ČáÁбí - ÊÔÌâÁбí
șț±±ÊĄ»„ÁȘÍű΄·šșÍČ»ÁŒĐĆÏąŸÙ±šÆœÌš | ÍűÉÏÓĐșŠĐĆÏąŸÙ±šŚšÇű | ”çĐĆŐ©ÆŸÙ±šŚšÇű | ÉæÀúÊ·ĐéÎȚÖśÒćÓĐșŠĐĆÏąŸÙ±šŚšÇű | ÉæÆóÇÖÈšŸÙ±šŚšÇű
΄·šșÍČ»ÁŒĐĆÏąŸÙ±š”ç»°Łș027-86699610 ŸÙ±šÓÊÏäŁș58377363@163.com