
| A. | 邻二甲苯、间二甲苯、对二甲苯沸点依次减小 | |
| B. | 蛋白质溶液加双缩脉试剂会显紫玫瑰色,与茚三酮溶液共热会显蓝紫色,与浓硝酸微热会产生黄色固体 | |
| C. | 在有机物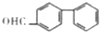 中至少有14个原子共平面 中至少有14个原子共平面 | |
| D. | 1.0mol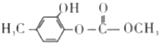 最多能与含3.0mol NaOH的水溶液完全反应 最多能与含3.0mol NaOH的水溶液完全反应 |
分析 A.依据苯的同分异构体沸点规律:对称性越好沸点越低;
B.蛋白质溶液加双缩脉试剂会显紫玫瑰色,与茚三酮溶液共热会显蓝紫色;
C.苯是平面结构;
D.酯能与氢氧化钠反应发生水解,酚羟基能与氢氧化钠反应.
解答 解:A.对二甲苯>间二甲苯>邻二甲苯对称性依次减弱,依据称性越好沸点越低,沸点顺序为:对二甲苯<间二甲苯<邻二甲苯,故A正确;
B.蛋白质溶液加双缩脉试剂会显紫玫瑰色,与茚三酮溶液共热会显蓝紫色,与浓硝酸微热会产生黄色固体,故B正确;
C.苯是平面结构,有机物 中中间苯环上的碳原子和氢原子以及醛基上的碳原子和右边苯环上的碳、对位上的碳原子及氢原子,至少有14个原子共平面,故C正确;
中中间苯环上的碳原子和氢原子以及醛基上的碳原子和右边苯环上的碳、对位上的碳原子及氢原子,至少有14个原子共平面,故C正确;
D.酯能与氢氧化钠反应发生水解,酚羟基能与氢氧化钠反应,1.0mol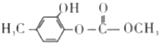 最多能与含4.0mol NaOH的水溶液完全反应,故D错误.
最多能与含4.0mol NaOH的水溶液完全反应,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握常见有机物的组成、官能团与性质的关系等为解答的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B的物质的量浓度 | D. | 气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
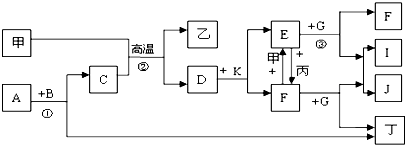
 、甲在周期表中位置是第四周期第Ⅷ族;
、甲在周期表中位置是第四周期第Ⅷ族;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
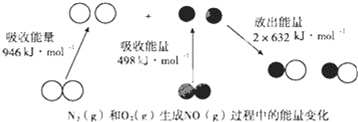
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com