
| A. | 生成了一种强酸弱碱盐 | B. | 弱酸溶液和强碱溶液反应 | ||
| C. | 强酸溶液和弱碱溶液反应 | D. | 一元强酸溶液和一元强碱溶液 |
分析 常温下pH=3的酸和pH=11的碱溶液等体积混合,混合溶液呈酸性,可能是酸为弱酸、碱为强碱,混合后酸后剩余;也可能是酸、碱都是弱电解质,但酸的电离程度小于碱的电离程度,据此分析解答.
解答 解:常温下,若将pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,可能是酸为弱酸、碱为强碱,混合后酸后剩余;也可能是酸、碱都是弱电解质,但酸的电离程度小于碱的电离程度,
A.混合溶液呈酸性,可能是酸为弱酸、碱为强碱或弱碱,生成的盐可能是强碱弱酸盐或弱酸弱碱盐,故A错误;
B.如果酸是弱酸、碱为强碱,二者混合后酸有剩余,酸的电离程度大于其酸根离子水解程度而导致溶液呈酸性,故B正确;
C.如果酸是强酸、碱是弱碱,二者混合后碱有剩余,溶液应该呈碱性,故C错误;
D.如果是一元强酸和一元强碱混合,二者物质的量相等,二者恰好反应生成强酸强碱盐,其溶液呈中性,与题意不符,故D错误;
故选B.
点评 本题考查酸碱混合溶液定性判断,正确理解题给信息是解本题关键,根据混合溶液酸碱性判断酸、碱强弱,易错选项是A.


科目:高中化学 来源: 题型:多选题
| A. | 实验中所用到的滴定管、容量瓶,在使用前均需要检漏 | |
| B. | 如果实验中需用60mL 稀硫酸标准溶液,配制时应选用100ML容量瓶 | |
| C. | 容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小 | |
| D. | 酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大 | |
| E. | 配制溶液时,定容时俯视度数,则导致实验结果偏大 | |
| F. | 中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当A、B都是金属,A的还原性一定比B强 | |
| B. | 当A、B都是非金属时,A的非金属性一定比B强 | |
| C. | 当A是金属时,B可能是金属,也可能是非金属 | |
| D. | 当A是非金属时,B可能是非金属,也可能是金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,若溶液的pH=11,则Kb(NH3•H2O)=1×10-6 | |
| B. | 向溶液中加入少量CH3COONa固体,溶液中$\frac{c(N{H}_{3}.{H}_{2}O)}{c(N{H}_{4}^{+})}$的值变小 | |
| C. | 向溶液中加入10 mL 0.1 mol•L-1盐酸,所得溶液中离子浓度大小顺序为:c(NH4+)>(Cl-)>c(H+)>c(OH-) | |
| D. | 向溶液中加入5 mL 0.1 mol•L-1盐酸,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ds区 | B. | d区 | C. | f区 | D. | s区和p区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的原子半径大于Y | |
| B. | 若X为ⅠA族元素,则该化合物中含离子键 | |
| C. | 若X2Y的焰色为黄色,则它的电子式是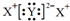 | |
| D. | 若每个X2Y分子中含有10个电子,则Y是第3周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
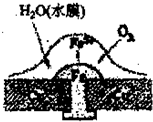 铜板上鉄柳钉若较长时间地浸泡在海水中会生锈甚至腐烂,其腐蚀远离如图所示,下列有关此过程的说法不正确的是( )
铜板上鉄柳钉若较长时间地浸泡在海水中会生锈甚至腐烂,其腐蚀远离如图所示,下列有关此过程的说法不正确的是( )| A. | 正极上的主要电极反应式:2H2O+O2+4e-→4OH- | |
| B. | 此过程中铜并未被腐蚀 | |
| C. | 电子从Cu流向Fe | |
| D. | 此过程中还可能涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com