
【题目】在温度为T时,向2.0 L恒容密闭容器中充入1.0 molA和1.0 molB,发生反应A(g)+B(g)![]() C(g),一段时间后达到平衡。测定得部分数据见下表:
C(g),一段时间后达到平衡。测定得部分数据见下表:
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
(1)反应前5 s的平均反应速率v(A)=____________。
(2)温度为T时,达到平衡后B物质的量的浓度=________。
(3)升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH_______0(填“>”或“<”)。
(4)下列措施能增大反应速率,且平衡向正反应方向移动是__________。
a.及时分离出A气体 b.适当升高温度 c.增大B的浓度 d.选择高效催化剂
【答案】0.015 mol/(L·s)0.4mol/L<c
【解析】
(1)根据表格数据,反应在前5s的A的物质的量变化为0.15mol,根据公式v=△n/V△t计算,平均速率V(A)= 0.15/(2×5)=0.015 mol/(L·s);正确答案:0.015 mol/(L·s)。
(2)由表中数据可知,反应在25s、35s时A的物质的量相等,说明25s时达到了平衡状态,则:
A(g) + B(g)![]() C(g)
C(g)
反应前(mol) 1.0 1.0 0
变化(mol) 0.2 0.2 0.2
平衡时(mol) 0.8 0.8 0.2
平衡时B的浓度为:c(B)= 0.8mol/2L =0.4mol/L;正确答案:0.4mol/L。
(3)根据题给数据分析,反应达平衡时c(A)=0.4mol/L,保持其他条件不变,升高温度,平衡时c(A)=0.41mo1· L-1,说明平衡逆向移动,升高温度平衡向吸热反应方向移动,正向放热△H<0;正确答案:<。
(4)a.分离出A气体,反应物浓度减小,正速率减小,逆反应速率瞬间不变然后减小,平衡向逆反应方向移动,错误;
b.升高温度,正、逆反应速率都增大,逆反应速率增大更多,平衡向逆反应方向移动,错误;
c.增大B的浓度,反应速率都增大,平衡正反应方向移动,正确;
d.催化剂同等程度的增大正、逆反应速率,平衡不移动,错误;
正确选项c。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】硫铁矿烧渣的主要成分为 Fe2O3、Fe3O4,以及少量 SiO2、Al2O3 等。由硫铁矿烧渣制备铁红(Fe2O3) 的一种工艺流程如下:

已知:还原焙烧时,大部分 Fe2O3、Fe3O4 转化为 FeO。 几种离子开始沉淀和完全沉淀时的 pH 如下表所示:

(1) “酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)______________。
(2)Fe 粉除调 pH 外,另一作用是___________;Fe 粉调节溶液的 pH 范围为__________。
(3) 已知“沉铁、过滤”中生成沉淀为碳酸铁沉淀,则高温条件下,“氧化”步骤中发生反应的化学方程式为______________。
(4) Fe2O3 也是赤铁矿的主要成分,工业上若要得到 120t 纯度为 93%生铁需要含杂质 20%的(杂质不含铁 元素)赤铁矿的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式为:2Fe3++Fe![]() 3Fe2+,能实现该反应的原电池是
3Fe2+,能实现该反应的原电池是
A. 正极为Cu,负极为Fe,电解质为FeCl3溶液
B. 正极为C,负极为Fe,电解质为FeSO4溶液
C. 正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液
D. 正极为Ag,负极为Cu,电解质为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅与氢氧化钠溶液反应(Si+2NaOH+H2O=Na2SiO3+2H2↑)的说法正确的是( )
A.氧化剂是NaOH和H2OB.氧化剂是H2O
C.氧化剂是SiD.还原剂是H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制下列四种无色透明的酸性溶液,其中能配制成功的是
A.NH4+、NO3-、Al3+、Cl-B.Na+、Fe3+、OH-、NO3-
C.MnO4-、K+、SO42-、Na+D.Ca2+、Mg2+、HCO3-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:

(1)该反应为____反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是____(填字母)。
A.改铁片为铁粉 B.滴加少量CuSO4 溶液
C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_______极(填“正”或“负”)。铜片上产生的现象为________,该极上发生的电极反应为_______。2min后铁片的质量减少1.4 g,则导线中流过的电子为____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:
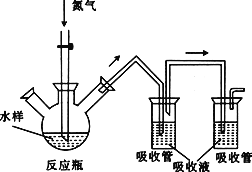
Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知:![]() )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。

(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是
A. HSO3-+ H2O![]() SO32- + OH- B. Al3+ + 3H2O == 3H+ + Al(OH)3↓
SO32- + OH- B. Al3+ + 3H2O == 3H+ + Al(OH)3↓
C. NaHCO3 == Na+ + HCO3- D. H2S![]() 2H+ + S2-
2H+ + S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) ΔH=+550 kJ·mol-1
它由两步反应组成:i. H2SO4(l)=SO3(g)+H2O(g) ΔH=+177 kJ·mol-1 ii. SO3(g)分解。
L(L1、L2)、X可分别代表压强和温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。

① X代表的物理量是_____________________。
② 判断L1、L2的大小关系是______________。
(2)反应Ⅱ:I-可以作为催化剂,可能的催化过程如下。
i. SO2+4I-+4H+=S↓+2I2+2H2O; ii. I2+2H2O+ SO2= SO42-+4H++2I-;
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol/L KI | a mol/LKI 0.2 mol/LH2SO4 | 0.2 mol/L H2SO4 | 0.2 mol/L KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
① B是A的对比实验,则a=__________。
② 比较A、B、C,可得出的结论是_______________________________。
③ 实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:___________。
(3)在钠碱循环法中,Na2SO3溶液作为吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:

① 上表判断NaHSO3溶液显__________性,用化学平衡原理解释:_____________。
② HSO3-在阳极放电的电极反应式是______,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com