
| A. | S2-+Cl2═S↓+2Cl- | B. | S2-+2Br-+2Cl2═S↓+Br2+4Cl- | ||
| C. | 2S2-+2Br-+3Cl2═2S↓+Br2+6Cl- | D. | 3S2-+2Br-+4Cl2═3S↓+Br2+8Cl- |
分析 还原性硫离子大于溴离子,通入氯气先发生Na2S+Cl2═2NaCl+S↓、氯气足量再氧化NaBr,结合氧化的先后顺序及电子守恒解答.
解答 解:A.氯气少量时发生S2-+Cl2═S↓+2Cl-,故A正确;
B.S2-+2Br-+2Cl2═S↓+Br2+4Cl-中不符合等物质的量浓度的Na2S和NaBr,故B错误;
C.氯气足量时发生2S2-+2Br-+3Cl2═2S↓+Br2+6Cl-,故C正确;
D.氯气足量时且溴离子部分氧化发生3S2-+2Br-+4Cl2═3S↓+Br2+8Cl-,故D正确;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握物质的性质、发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意氧化的先后顺序及离子反应中电子、电荷守恒,题目难度不大.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:实验题
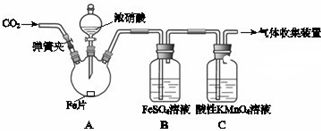
| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuCl2 | B. | CuSO4 | C. | Cu(OH)2 | D. | CuCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
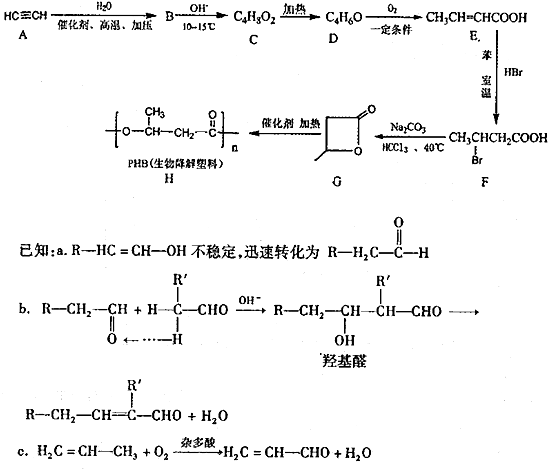
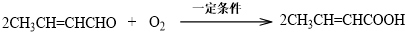 .
.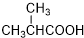 .
.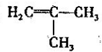 为起始原料(其他原料任选),制备
为起始原料(其他原料任选),制备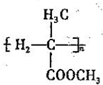 的合成路线:
的合成路线: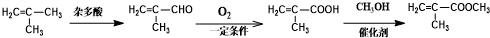
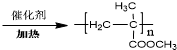 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
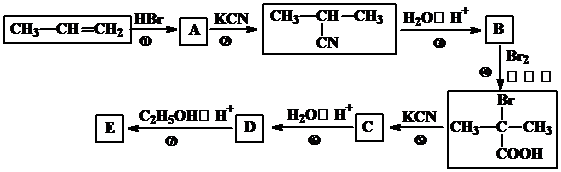
 .
. +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.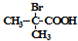 与足量NaOH乙醇溶液反应的化学方程式为
与足量NaOH乙醇溶液反应的化学方程式为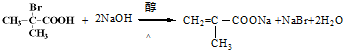 .
. 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com