
| A、钢铁制品腐蚀时正极反应:O2+2H2O+4e-=4OH- |
| B、在酸性较强的溶液中,金属主要发生析氢腐蚀 |
| C、为减缓金属腐蚀,可将要保护的金属物件与外电源的正极相连接 |
| D、在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、
| ||
| B、1mol | ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液氨可用做致冷剂,碱石灰可用于干燥氨气 |
| B、铁制器皿可用于盛放稀硫酸 |
| C、小苏打可用于治疗胃酸过多 |
| D、氯气可用于自来水消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大NO2的浓度,平衡常数增大 |
| B、增大N2O4的浓度,平衡常数增大 |
| C、增大NO2的浓度,正反应速率加快,逆反应速率减慢 |
| D、增大NO2的浓度,平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
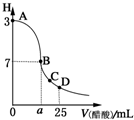 在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )
在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )| A、在D点,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、在C点,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、在B点,a=12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 |
| B、在原电池装置中,电子从负极流出,沿导线流入正极,经溶液或盐桥回到负极 |
| C、在c(H+)/c(OH-)=l012溶液中 Na+、I-、NO3-、SO42-不能大量共存 |
| D、饱和FeCl3溶液在20℃时呈现棕黄色,100℃呈现红褐色,不能用平衡移动原理来解释 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知20℃时,KNO3的溶解度为31.6g.则20℃时KNO3饱和溶液的质量分数等于31.6% |
| B、1mol/L的食盐溶液中含有58.5gNaCl |
| C、所有物质的溶解度随着温度的升高而上升 |
| D、实验室需要230mL 0.1mol/L的H2SO4溶液,应选用250mL容量瓶配制 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com