
【题目】如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题: 
(1)该浓盐酸中HCl的物质的量浓度为 . 若用KMnO4氧化上述 HCl.其反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(2)1mol KMnO4完全反应,反应后溶液的体积为2L,则所得产物中Cl﹣的物质的量浓度为
(3)8mol HCl完全反应,产生的Cl2在标准状况下的体积为 .
【答案】
(1)11.9mol/L
(2)1.5mol/L
(3)56L
【解析】解:(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度= ![]() =11.9mol/L, 所以答案是:11.9;
=11.9mol/L, 所以答案是:11.9;
·(2)
2KMnO4+ | 16HCl(浓) | = | 2KCl+ | 2MnCl2+ | 5Cl2↑+ | 8H2O |
2 | 2 | 2 | ||||
1mol | 1mol | 1mol |
所得产物中Cl﹣的物质的量n(Cl﹣)=n(KCl)+2n(MnCl2)=1mol+2mol=3mol,则所得产物中Cl﹣的物质的量浓度为 ![]() =1.5mol/L,
=1.5mol/L,
所以答案是:1.5mol/L;
·(3)8mol HCl完全反应,令生成的氯气的物质的量为x,则:
2KMnO4+ | 16HCl(浓) | = | 2KCl+ | 2MnCl2+ | 5Cl2↑+ | 8H2O |
16 | 5 | |||||
8mol | x |
故x= ![]() =2.5mol,故氯气的体积为2.5mol×22.4L/mol=56L,
=2.5mol,故氯气的体积为2.5mol×22.4L/mol=56L,
所以答案是:56L.


科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.原子的核外电子层数等于该元素所在的周期数
B.元素周期表中从IIIB族到IIB族10个纵行的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8
D.同一元素的各种同位素的物理性质、化学性质均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.硫粉在过量的氧气中燃烧可以生成SO3
B.可以用澄清石灰水鉴别CO2和SO2
C.将少量CO2通入BaCl2溶液能生成白色沉淀
D.不能用排水法收集SO2、NO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则①电解池中X极上的电极反应式为 . 在X极附近观察到的实验现象是 . ②Y电极上的电极反应式为 .
③要使电解后溶液恢复到电解前的状态,则需加入(或通入) .
(2)如果要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则: ①X电极的材料是 , 电极反应式为 .
②Y电极的材料是 , 电极反应式为 . (说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向400mL 稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出 NO气体 8.96L(标准状况),同时溶液质量增加 13.2g。下列判断正确的是
A. 反应后的溶液中 c(Fe2+)︰c(Fe3+) =1︰2
B. 原溶液中投入铁粉物质的量是 0.4 mol
C. 原溶液中 HNO3 的浓度是 4.0 mol/L
D. 反应后的溶液中还可溶解 4.8g 铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。

(1)反应Ⅰ的离子方程式为_____________,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得到AgCl固体1.435g;
③另取25.00mL溶液A,调节pH为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00mL。通过计算确定该样品的化学式为___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中常用氧化浓盐酸的方法制取氯气,实验装置如图所示:
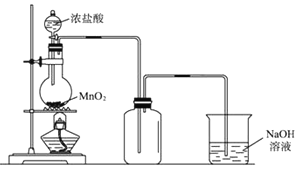
(1)写出制备氯气的离子方程式: ______ ;
(2)为了得到纯净、干燥的氯气,此装置还需增加净化装置,请根据气体的流动方向,依次按顺序选择所用的装置,正确的选项是 ______ ;
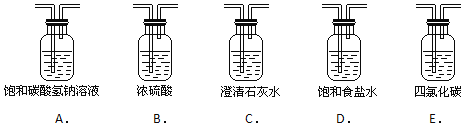
(3)如果将过量二氧化锰与20mL12mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有:① ______ ;② ______ .
(4)多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置 ______ ;
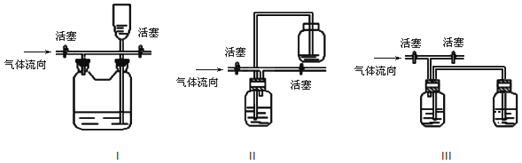
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物,常温常压下,p为无色无味气体,q为液态,r为淡黄色固体,s是气体单质。上述物质的转化关系如下图所示。下列说法错误的是

A. 原子半径:Z>Y>X
B. 最简单气态氢化物的稳定性:Y>X
C. m、n、r都含有离子键和共价键
D. m、n、t都能破坏水的电离平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com