
(12分)下图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下的气态化合物,C为常温下的液态化合物,图中有部分生成物未标出。
请填写以下空白:

(1)A的化学式为 ,B的电子式为 。
(2)写出下列反应的化学方程式:
D+G→H 。
F+J→B+C+I 。
(3)0.3 mol I与足量C反应转移电子的物质的量为 mol。
(4)容积为10 mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I与G的体积分别为 mL, mL。
(1) NH4HCO3(2分),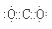 (2分)
(2分)
(2)4NH3+5O2 4NO+6H2O (2分) C+4HNO3(浓)
4NO+6H2O (2分) C+4HNO3(浓) 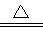 =CO2↑+4NO2↑+2H2O(2分)
=CO2↑+4NO2↑+2H2O(2分)
(3)0.2(2分)
(4)8(1分)2(1分)
【解析】
试题分析:(1)已知A分解得到等物质的量的B、C、D,分析反应特点判断A是碳酸氢铵,化学式为NH4HCO3,镁条在B中燃烧,说明B是二氧化碳,则B的电子式为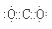 ;
;
(2)铵盐与碱共热得D为氨气,过氧化钠与水反应生成G氧气,所以氨气与氧气的催化氧化反应的化学方程式为4NH3+5O2 4NO+6H2O ;J为硝酸,F为碳单质,所以F+J→B+C+I的化学方程式为C+4HNO3(浓)
4NO+6H2O ;J为硝酸,F为碳单质,所以F+J→B+C+I的化学方程式为C+4HNO3(浓)  =CO2↑+4NO2↑+2H2O(2分);
=CO2↑+4NO2↑+2H2O(2分);
(3)I为NO2,与水的反应:3NO2+H2O=2HNO3+NO既作氧化剂又作还原剂,所以0.3mol的NO2与水的反应中转移电子的物质的量是0.2mol,
(4)NO2与O2恰好反应时物质的量之比是4:1,所以10mL混合气体中有8mL NO2,2mL O2
考点:考查物质推断,电子式、化学方程式的书写,氧化还原反应的计算


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014学年辽宁省东北三省高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
下图是某企业设计的硫酸—磷肥—水泥联产、海水—淡水多用、盐—热—电联产的三大生态产业链流程图。

根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:① 、② 、③ 、④ 、⑤ 。
(2)沸腾炉发生反应的化学方程式: 。磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙得化学方程式 。
(3)用1吨硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸 吨。
(4)热电厂的冷却水是 ,该流程中浓缩盐水除提取盐以外还可提取的物质有 (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。
, (写出两点即可)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年甘肃省张掖市高三第三次诊断考试理综化学试卷(解析版) 题型:选择题
人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农业生产及日常生活方面用途非常广泛。试回答下列问题。
(1)Cu+的核外电子排布式为 。
(2)铜镁合金是一种储氢材料,某种铜镁互化物晶胞结构如图,则该互化物的化学式为 。

(3)叠氮化铜[Cu(N3)2]是一种紫黑色粉末,易爆炸,与N3-互为等电子体的分子有 (举2例)。
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO OHC-CH2CH2OH。
OHC-CH2CH2OH。
OHC-CH2CH2OH中碳原子杂化方式有 ,乙炔属于 (填“极性”或“非极性”)分子。
(5)若向盛有CuSO4溶液的试管里加入氨水,首先形成蓝色难溶物,继续加入氨水,难溶物溶解,变成蓝色透明溶液,这时得到一种称为硫酸四氨合铜的物质,该物质的化学式为______________,其中含有的化学键类型有 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省益阳市高三下学期模拟考试理综化学试卷(解析版) 题型:选择题
下列实验操作不能达到实验目的的是
| 实验目的 | 实验操作 |
A | 证明乙烯能发生加成反应 | 将乙烯气体通入溴的四氯化碳溶液中 |
B | 鉴别Fe(OH)3胶体和FeCl3溶液 | 用激光笔分别照射两种物质,从侧面观察是否出现光亮的通路。 |
C | 检验酒精中是否含有水 | 取少量酒精加入无水硫酸铜粉末 |
D | 鉴别苯、环已烯和已烷 | 加入酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:填空题
肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体。
(1)肉桂酸甲酯由C、H、O三种元素组成,质谱分析其分子的相对分子质量为162,核磁共振氢谱谱图显示有6个峰,其面积之比为1:2:2:1:1:3,利用红外光谱仪检测其中的某些基团,测得红外光谱如下图:

则肉桂酸甲酯的结构简式是 (不考虑立体异构)
(2)已知:
I.醛与醛能发生反应,原理如下:

Ⅱ.已知烃A在标准状况下的密度为1.25g.L-1。合成肉桂酸甲酯的工业流程如下图所示:

请回答:
①化合物J的结构简式为 ;
②化合物G中的官能团有 ;
③G→H为 反应(填反应类型);
④写出反应D→E的化学方程式 ;
H→I的反应 (填“能”或“不能”)改用酸性高锰酸钾溶液,简述理由: 。
⑤符合下列条件的I的同分异构体共有5种。写出另两种同分异构体的结构简式:
A.能发生水解反应
B.与银氨溶液作用出现光亮的银镜
C.能与溴发生加成

查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省十三校高三第二次联考理综化学试卷(解析版) 题型:选择题
短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,元素D位于第ⅥA族。下列说法正确的是
A.原子半径:D>B>C>A
B.元素A、B的氧化物所含化学键的类型完全相同
C.元素B和C的最高价氧化物对应水化物的碱性:B<C
D.元素B、C、D的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省天门市毕业生四月调研测试理综化学试卷(解析版) 题型:填空题
Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:

(1)该合成路线对于环境保护的价值在于 。
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因 。
(3)CH3OH、H2的燃烧热分别为:△H=-725.5 kJ/mol、△H=-285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g)  CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
1.5 | 45% | 33% | 20% | 12% |
2.0 | 60% | 43% | 28% | 15% |
3.0 | 83% | 62% | 37% | 22% |
(4)该反应的焓变△H 0,熵变△S 0(填>、<或=)。
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。
(6)若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河南省商丘市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v(正)>v(逆)
D.80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省南昌市高三3月第一次模拟考试理综化学试卷(解析版) 题型:选择题
若两物质恰好完全反应,下列各项中反应前后保持不变的是
①电子总数;②原子总数;③分子总数;④物质的总能量;⑤物质的总质量
A.①②⑤ B.①③⑤ C.②③④ D.②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com