
| A. | 11.2L NH3中含有的氢原子数为1.5NA | |
| B. | 0.2mol/L AlCl3溶液含有0.2NA个Al3+ | |
| C. | 常温常压下,18g水的原子数为3NA | |
| D. | O2与O3的混合物32g,含有分子数为NA |
分析 A、氨气所处的状态不明确;
B、溶液体积不明确;
C、求出水的物质的量,然后根据1mol水中含3mol原子来分析;
D、氧气和臭氧的摩尔质量不同.
解答 解:A、氨气所处的状态不明确,故无法计算其物质的量,故A错误;
B、溶液体积不明确,故溶液中的铝离子的个数无法计算,故B错误;
C、18g水的物质的量为1mol,而1mol水中含3mol原子,即3NA个,故C正确;
D、氧气和臭氧的摩尔质量不同,分别为32g/mol和46g/mol,故32g混合物的物质的量介于1mol~$\frac{2}{3}$mol,即分子数介于NA~$\frac{2}{3}$NA,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 柠檬属于酸性食物 | |
| B. | 油脂是人类维持生命活动所需能量的主要来源 | |
| C. | PM2.5是指空气中氮氧化物和硫氧化物含量之和 | |
| D. | 登高山时防晒是为了防止强紫外线引起皮肤蛋白质被灼伤变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 实验操作 | 实验现象 |
| 甲 | ①取少量粉末,加入过量浓硝酸 ②向上述溶液中加入几滴NaCl溶液 | 粉末溶解,有红棕色气体产生 有白色沉淀生成 |
| 乙 | ③取少量粉末,加入足量NaOH溶液 ④向上述溶液中逐滴加入稀盐酸 ⑤继续加入过量的稀盐酸 | 粉末溶解,有气泡产生 有白色沉淀生成 白色沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应必然伴随能量的变化 | |
| B. | 我国目前使用的主要能源是化石能源 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 化学反应一定有化学键的断裂与形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
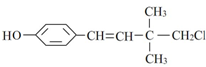 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 有顺反异构 | |
| B. | 可以和浓溴水发生取代反应和加成反应 | |
| C. | 可以发生加聚反应、水解反应和消去反应 | |
| D. | 1mol该化合物最多能与4 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol 18O含有的中子数为10NA | |
| B. | 22.4L甲烷气体中所含分子数目为NA | |
| C. | 1L 0.1mol•L-1NH4Cl 溶液中NH4+数目为 0.1NA | |
| D. | 1L pH=1的醋酸溶液中,CH3COOH分子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制FeSO4溶液时,加入一些铁粉 | |
| B. | 500℃左右比室温更有利于合成氨的反应 | |
| C. | 实验室常用排饱和食盐水的方法收集氯气 | |
| D. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,容器体积扩大一倍,A的浓度是原来的0.45倍,则a+b>c+d | |
| B. | 若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为b:a | |
| C. | 若平衡体系中共有气体n mol,再向其中充入bmolB,达到平衡时气体总物质的量为n+bmol,则a+b=c+d | |
| D. | 若a+b=c+d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com