
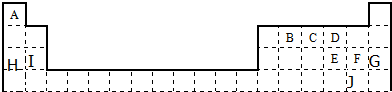
 ŅŃÖŖV”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅ»“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬V”¢YŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČē±ķĖłŹ¾£¬VŌŖĖŲÓėŃõŌŖĖŲÄÜŠĪ³ÉĮ½ÖÖĪŽÉ«ĘųĢ壬XŹĒµŲæĒÖŠŗ¬Įæ×ļĖłµÄ½šŹōŌŖĖŲ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŅŃÖŖV”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅ»“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬V”¢YŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČē±ķĖłŹ¾£¬VŌŖĖŲÓėŃõŌŖĖŲÄÜŠĪ³ÉĮ½ÖÖĪŽÉ«ĘųĢ壬XŹĒµŲæĒÖŠŗ¬Įæ×ļĖłµÄ½šŹōŌŖĖŲ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö V”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬XŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ£¬ŌņXŹĒAlŌŖĖŲ£»V”¢YŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼£¬øł¾ŻĶ¼ÖŖ£¬VĪŖµŚ¶žÖÜĘŚŌŖĖŲ£¬VŌŖĖŲÓėŃõŌŖĖŲÄÜŠĪ³ÉĮ½ÖÖĪŽÉ«ĘųĢ壬ŌņVŹĒCŌŖĖŲ”¢YŹĒSŌŖĖŲ£»ZµÄŌ×ÓŠņŹż“óÓŚSŌŖĖŲĒŅĪŖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĖłŅŌZŹĒClŌŖĖŲ£¬£Ø3£©ÖŠWµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļ¼×µÄĖ®ČÜŅŗĻŌ¼īŠŌ£¬ŌņWŹĒNŌŖĖŲ£¬¼×ŹĒ°±Ęų£¬
£Ø1£©ZĪŖClŌŖĖŲ£¬ĘäŌ×ÓŠņŹżĪŖ17£¬×īĶā²ćĪŖ7øöµē×Ó£»
£Ø2£©SO2ĘųĢåĶØČėBaCl2ŗĶHNO3µÄ»ģŗĻČÜŅŗ£¬Éś³É°×É«³ĮµķŗĶĪŽÉ«ĘųĢåNO£¬·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĮņĖįøłĄė×ÓŗĶNO£¬ĮņĖįøłĄė×ÓŗĶ±µĄė×Ó·“Ӧɜ³ÉĮņĖį±µ°×É«³Įµķ£»Ķ¬Ņ»Ńõ»Æ»¹Ō·“Ó¦ÖŠ»¹Ō¼ĮµÄ»¹ŌŠŌ“óÓŚ»¹Ō²śĪļµÄ»¹ŌŠŌ£»
£Ø3£©°±ĘųŗĶĖ«ŃõĖ®·“Ó¦µÄ²śĪļ²»ĪŪČ¾»·¾³£¬Ó¦Éś³ÉµŖĘųŗĶĖ®£®
½ā“š ½ā£ŗV”¢W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬XŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ£¬ŌņXŹĒAlŌŖĖŲ£»V”¢YŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼£¬øł¾ŻĶ¼ÖŖ£¬VĪŖµŚ¶žÖÜĘŚŌŖĖŲ£¬VŌŖĖŲÓėŃõŌŖĖŲÄÜŠĪ³ÉĮ½ÖÖĪŽÉ«ĘųĢ壬ŌņVŹĒCŌŖĖŲ”¢YŹĒSŌŖĖŲ£»ZµÄŌ×ÓŠņŹż“óÓŚSŌŖĖŲĒŅĪŖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĖłŅŌZŹĒClŌŖĖŲ£¬£Ø3£©ÖŠWµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļ¼×µÄĖ®ČÜŅŗĻŌ¼īŠŌ£¬ŌņWŹĒNŌŖĖŲ£¬¼×ŹĒ°±Ęų£¬
£Ø1£©ZŹĒClŌŖĖŲ£¬ĘäŌ×Ó×īĶā²ćÓŠ7øöµē×Ó”¢3øöµē×Ó²ć£¬Ī»ÓŚÖÜĘŚ±ķÖŠµŚČżÖÜĘŚµŚVIIA×壬
¹Ź“š°øĪŖ£ŗµŚČżÖÜĘŚµŚVIIA×壻
£Ø2£©SO2ĘųĢåĶØČėBaCl2ŗĶHNO3µÄ»ģŗĻČÜŅŗ£¬Éś³É°×É«³ĮµķŗĶĪŽÉ«ĘųĢåNO£¬·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĮņĖįøłĄė×ÓŗĶNO£¬ĮņĖįøłĄė×ÓŗĶ±µĄė×Ó·“Ӧɜ³ÉĮņĖį±µ°×É«³Įµķ£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ3SO2+2NO3-+3Ba2++2H2O=3BaSO4”ż+2NO+4H+£»Ķ¬Ņ»Ńõ»Æ»¹Ō·“Ó¦ÖŠ»¹Ō¼ĮµÄ»¹ŌŠŌ“óÓŚ»¹Ō²śĪļµÄ»¹ŌŠŌ£¬øĆ·“Ó¦ÖŠSO2ŹĒ»¹Ō¼Į”¢NOŹĒ»¹Ō²śĪļ£¬ĖłŅŌ¶žŃõ»ÆĮņµÄ»¹ŌŠŌ½ĻĒ棬¼“»¹ŌŠŌ£ŗSO2£¾NO£¬
¹Ź“š°øĪŖ£ŗ3SO2+2NO3-+3Ba2++2H2O=3BaSO4”ż+2NO+4H+£»SO2£¾NO£»
£Ø3£©°±ĘųŗĶĖ«ŃõĖ®·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉµŖĘųŗĶĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ2NH3+3H2O2=N2+6H2O£¬¹Ź“š°øĪŖ£ŗ2NH3+3H2O2=N2+6H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪ»ÖĆ½į¹¹ÓėŠŌÖŹ¹ŲĻµµÄÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£¬ÕżČ·ĶʶĻø÷ŌŖĖŲĆū³ĘĪŖ½ā“š¹Ų¼ü£¬×¢ŅāŹģĮ·ÕĘĪÕŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ”¢ŌŖĖŲÖÜĘŚ±ķµÄ¹ŲĻµ£¬ŹŌĢā²ąÖŲæ¼²éѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄʵĵē×ÓŹ½£ŗ | |
| B£® | ¾ŪĀČŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗ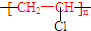 | |
| C£® | ĮņĄė×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ | |
| D£® | Ģ¼ĖįĒāļ§µÄµēĄė·½³ĢŹ½£ŗNH4HCO3=NH4++H++CO32”„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molNa2O2ÖŠŗ¬ÓŠµÄĄė×Ó×ÜŹżĪŖ4 NA | |
| B£® | 0.1 molōĒ»ł£Ø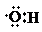 £©ÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ0.7 NA £©ÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ0.7 NA | |
| C£® | ŹŅĪĀĻĀ£¬1 L pH=13µÄNaOHČÜŅŗÖŠ£¬Ė®µēĄė³öµÄOH-µÄŹżÄæĪŖ0.1 NA | |
| D£® | ŌŚ5NH4NO3$\frac{\underline{\;\;”÷\;\;}}{\;}$2HNO3+4N2”ü+9H2OÖŠ£¬Éś³É28 g N2Ź±×ŖŅʵĵē×ÓŹżÄæĪŖ3.75 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ī¢Į£ | A | B | C | D |
| Ō×ÓŗĖŹż | Ė«ŗĖ | ¶ąŗĖ | ¶ąŗĖ | ¶ąŗĖ |
| Ėł“ųµ„Ī»µēŗÉ | -1 | 0 | +1 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć÷·ÆæÉÓĆÓŚ×ŌĄ“Ė®µÄĻū¶¾¾»»Æ | |
| B£® | Fe2 O3æÉÓĆ×÷ŗģÉ«ÓĶĘįŗĶĶæĮĻ | |
| C£® | ·ÓČ©Ź÷Ö¬æÉÓĆ×÷¾ųŌµ”¢øōČČŗĶø“ŗĻ²ÄĮĻ | |
| D£® | ĮņĖįæÉÓĆÓŚ¾«Į¶ŹÆÓĶŅŌ¼°ÖĘČ”¶ąÖÖ»Ó·¢ŠŌĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com