
【题目】工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是__(填字母序号)。
a.![]() b.
b.![]()
c.![]() d.
d.![]()
(2)写出CO的一种常见等电子体的结构式:___;C、N、O的第一电离能由大到小的顺序为__(用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是___。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,1mol[Cu(NH3)2]+中含有σ键的数目___。则其中碳原子的杂化轨道类型是__,NH3分子的价电子对互斥理论模型是___。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
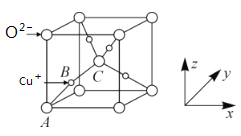
①若坐标参数A为(0,0,0),B为(![]() ,
,![]() ,
,![]() ),则C的坐标参数为__;
),则C的坐标参数为__;
②若阿伏加德罗常数为NA,该晶胞的边长为apm,则晶体的密度为___gcm-3。
【答案】a N≡N N>O>C H2Te、H2Se、H2S均是分子晶体,相对分子质量逐渐减小,范德华力减小,所以沸点减小,而水分子中存在氢键,所以沸点最高 8NA sp3、sp2 四面体形 (![]() ,
,![]() ,
,![]() )
) ![]()
【解析】
(1)根据基态原子核外电子排布进行判断,基态排布为能量最低的排布;
(2)等电子体为原子总数相同,价电子总数也相同的微粒;
(3)沸点与范德华力和氢键的有关;
(4)根据结构和价电子互斥理论进行计算;
(5)根据晶胞结构和晶体密度方程回答问题。
(1)基态N的核外电子排布式为1s22s22p3,基态排布为能量最低的排布,电子排布图表示的状态中只有a项符合;
(2)等电子体为原子总数相同,价电子总数也相同的微粒,与CO互为等电子体的一种分子为N2,其结构式为:N≡N;同周期主族元素,随着原子序数增大,第一电离能呈增大的趋势,但第ⅤA族元素其价电子排布为ns2np3,其np中电子排布为半满结构,较稳定,因此其第一电离能比相邻元素大,所以C、N、O的第一电离能由大到小的顺序为:N>O>C;
(3)H2Te、H2Se、H2S均是分子晶体,相对分子质量逐渐减小,范德华力减小,所以沸点减小,但由于氢键的作用力比范德华力强,氢键会使沸点异常升高,会导致H2O的沸点异常的高,所以沸点大小为H2O>H2Te>H2Se>H2S,故答案为:H2Te、H2Se、H2S均是分子晶体,相对分子质量逐渐减小,范德华力减小,所以沸点减小,而水分子中存在氢键,所以沸点最高;
(4)铜显+1价,1mol[Cu(NH3)2]+中N-H键和配位键属于σ键,即含有σ键的数目8NA,甲基中碳原子形成4个σ键,没有孤电子对,杂化轨道数目为4,碳原子杂化方式为sp3,而羰基中C原子形成3个σ键,没有孤电子对,杂化轨道数目为3,碳原子杂化方式为sp2;NH3中N原子形成3个N-H键,含有1对孤对电子,价层电子对数=3+1=4,价电子对互斥理论模型是四面体形,故答案为:sp3、sp2;四面体形;
(5)①根据晶胞结构分析,C位于晶胞体心,则C的原子坐标为:(![]() );
);
②1mol晶胞,即有NA个晶胞,质量为m=2×(64×2+16)g=144×2g,所以密度为ρ=![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1)将9.5gMgCl2溶于水配成1L溶液,所得溶液的物质的量浓度为___mol/L,500mL该溶液中所含Cl-的物质的量为___mol。
(2)含有2NA个氢原子的CH4的质量为___g。
(3)现有以下物质:①熔融NaCl ②液氨 ③醋酸水溶液 ④HCl气体 ⑤酒精(C2H5OH)。请用下列序号填空:能导电的是___(填选项);属于电解质的是___(填选项)。
A.①③ B.②④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组参照课文中的实验装置图做高温下铁与水蒸气反应的实验装置如图所示。在玻璃管中放入铁粉与石棉绒的混合物,加热,并通入水蒸气。用试管收集产生的干燥气体,并靠近火焰点火,观察现象。下列说法错误的是( )
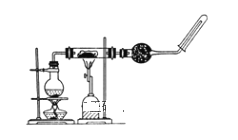
A.圆底烧瓶中盛装的是水,该装置受热后提供水蒸气
B.在圆底烧瓶内加入碎瓷片加快化学反应速率
C.实验时应先点燃酒精灯,后点燃酒精喷灯
D.石棉绒作铁粉的载体,防止铁粉被吹入导管而引起堵塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氟气反应生成氟化氢的过程中能量变化如图所示。由图可知

A. 生成1 molHF气体放出的热量为270 kJ
B. H2(g)+ F2(g)→ 2HF(l)+ 270 kJ
C. 反应物的总能量大于生成物的总能量
D. 该反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
Al | NaAlO2 | Al(OH)3 | Al2O3 | ||
② | Na | NaOH | Na2CO3 | NaCl | |
③ | C | CO | CO2 | H2CO3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①② B. ①③④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电溶氧化法从低品位钼矿中回收铼(Re),其原理如图所示,下列说法正确的是
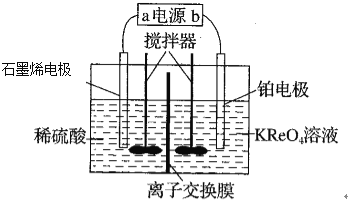
A.阴极材料选用石墨烯增大了接触面积
B.上图装罝中的离子交换膜为阴离子交换膜
C.铂电极反应式为8H++ReO4-+7e-=Re+4H2O
D.有0.4mole-转移时,石墨烯上产生0.2mo1H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物是工业上合成锅炉防腐剂的中间体,E(![]() )的一种合成路线如下:
)的一种合成路线如下:
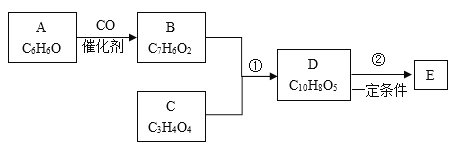
已知:
①R1CHO+R2CH2COOH![]() R1CH=CR2COOH;
R1CH=CR2COOH;
②RCH=C(COOH)2![]() RCH=CHCOOH+CO2
RCH=CHCOOH+CO2
回答下列问题:
(1)有机物A的化学名称为___________。
(2)1mol有机物C最多能与2molNaHCO3反应,C的结构简式为_____,有机物B中含有官能团的名称为_______。
(3)有机物D能发生的化学反应有____(填字母)。
a.加成反应b.消去反应c.水解反应d.氧化反应
(4)写出E在一定条件下生成聚酯的化学方程式:_______。
(5)有机物F分子比化合物B多了一个CH2原子闭,满足下列条件的F的同分异构体有_____种(不含立体异构),其中核磁共振氢谱为五组峰的物质的结构简式为_______。
①遇氯化铁溶液发生显色反应;②能发生银镜反应。
(6)已知:CH3CH=CH2+Cl2![]() ClCH2CH=CH2+HCl。以丙烯为原料(其他无机物任选)涉及制备化合物C的合成路线__________________________。
ClCH2CH=CH2+HCl。以丙烯为原料(其他无机物任选)涉及制备化合物C的合成路线__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)

(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com