
| A. | 1 mol 任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L水所含的H2O分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol钠失去电子的数目为2 NA个 |
分析 A.有的物质中不存在分子,如离子化合物、金属等;
B.氮气为双原子分子,1mol氮气中含有2mol氮原子;
C.标准状况下,水的状态不是气体;
D.钠为+1价金属,1mol钠完全反应失去1mol电子.
解答 解:A.1mol任何物质中不一定含有1mol分子,如1mol氯化钠、1mol铁等物质中都不存在分子,故A错误;
B.14g氮气的物质的量为:$\frac{14g}{28g/mol}$=0.5mol,0.5mol氮气中含有1mol氮原子,所含的N原子数为NA个,故B正确;
C.标况下水不是气体,不能使用标况下的气体摩尔体积计算,故C错误;
D.1mol钠完全反应最多失去1mol电子,失去电子的数目为NA个,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,能够辩别标况下常见物质状态.


科目:高中化学 来源: 题型:选择题
| A. | 若降低温度,可以加快反应速率 | |
| B. | 使用催化剂是为了加快反应速率 | |
| C. | 在上述条件下,N2的转化率能达到100% | |
| D. | 达到平衡时,N2、H2和NH3的浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂水解可得到丙三醇 | B. | 可用碘检验淀粉是否完全水解 | ||
| C. | 蛋白质水解的最终产物为氨基酸 | D. | 纤维素与淀粉互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
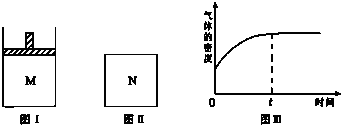
| A. | x=4 | |
| B. | 若N中气体的密度如图Ⅲ所示,则A、B都是气态 | |
| C. | 若A为气体,B为非气体,则平衡时M、N中C的物质的量相等 | |
| D. | 若A、B均为气体,平衡时M中A的转化率大于N中A的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2Al(s)+2NaOH(aq)+2H2O(1)═2NaAlO2(aq)+3H2(g);△H<O | |
| B. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq)+8H2O(1);△H>0 | |
| C. | C3H8(g)+5O2(g)→4H2O (l)+3CO2(g);△H<0 | |
| D. | FeCl3(aq)十3H2O(1)?Fe(OH)3(s)+3HCl(aq);△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-
(1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-查看答案和解析>>
科目:高中化学 来源: 题型:解答题
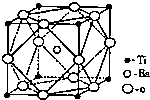 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入20g 固体NaOH,搅拌、溶解 | |
| B. | 将溶液加热浓缩至0.6 L | |
| C. | 加入10mol/L的NaOH溶液0.1 L,再稀释至1.5 L | |
| D. | 加入1 L 1.5 mol/L的NaOH溶液混合均匀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com