
ПВБРЛµ·ЁХэИ·µДКЗЈЁ Ј©
A.ГѕУлј«ПЎПхЛб·ґУ¦ЙъіЙПхЛб淋ДАлЧУ·ЅіМКЅОЄ:4Mg+6H++N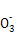 =4Mg2++N
=4Mg2++N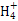 +3H2O
+3H2O
B.іЈОВПВ,0.1 mol/LТ»ФЄЛбHAИЬТєЦРc(OH-)/c(H+)=1ЎБ10-8,ФтґЛИЬТєµДpH=3
C.ПаН¬МхјюПВ,ЕЁ¶ИѕщОЄ0.01 mol/LµДNH4ClИЬТєєНNaClИЬТєЦР,З°ХЯµДСфАлЧУЧЬЕЁ¶ИґуУЪєуХЯµДСфАлЧУЧЬЕЁ¶И
D.ОпЦКµДБїЕЁ¶ИПаµИµДґЧЛбєНЗвСх»ЇДЖИЬТєµИМе»э»мєПєуµДИЬТєЦР:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(CH3COOH)
B
ЎѕЅвОцЎїAПоµзєЙЎўФЧУІ»КШєг,У¦ОЄ4Mg+10H++N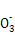 =4Mg2++N
=4Mg2++N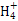 +3H2O,ґнОу;c(OH-)/c(H+)=1ЎБ10-8Улc(OH-)ЎБc(H+)=1ЎБ10-14БЄБў,їЙµГc(H+)=1ЎБ10-3 molЎ¤L-1,№КpH=3,B¶Ф;ёщѕЭИЬТєµзЦРРФ,NH4ClИЬТєЦРґжФЪc(N
+3H2O,ґнОу;c(OH-)/c(H+)=1ЎБ10-8Улc(OH-)ЎБc(H+)=1ЎБ10-14БЄБў,їЙµГc(H+)=1ЎБ10-3 molЎ¤L-1,№КpH=3,B¶Ф;ёщѕЭИЬТєµзЦРРФ,NH4ClИЬТєЦРґжФЪc(N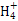 )+c(H+)=c(Cl-)+c(OH-),NaClИЬТєЦРґжФЪc(Na+)+c(H+)=c(Cl-)+c(OH-),УЙУЪNH4ClИЬТєПФЛбРФ¶шNaClИЬТєПФЦРРФ,јґЗ°ХЯµДc(OH-)РЎУЪєуХЯ,¶шc(Cl-)ѕщОЄ0.01 mol/L,№Кc(N
)+c(H+)=c(Cl-)+c(OH-),NaClИЬТєЦРґжФЪc(Na+)+c(H+)=c(Cl-)+c(OH-),УЙУЪNH4ClИЬТєПФЛбРФ¶шNaClИЬТєПФЦРРФ,јґЗ°ХЯµДc(OH-)РЎУЪєуХЯ,¶шc(Cl-)ѕщОЄ0.01 mol/L,№Кc(N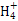 )+c(H+)Јјc(Na+)+c(H+),Cґн;ёщѕЭИЬТєµзЦРРФ,CH3COONaИЬТєЦРґжФЪc(Na+)+c(H+)=c(CH3COO-)+c(OH-),DґнЎЈ
)+c(H+)Јјc(Na+)+c(H+),Cґн;ёщѕЭИЬТєµзЦРРФ,CH3COONaИЬТєЦРґжФЪc(Na+)+c(H+)=c(CH3COO-)+c(OH-),DґнЎЈ



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§¶юВЦЧЁМвН»ЖЖ ЧЁМвИэИЬТєЧйіЙµДјЖБїј°ЖдУ¦УГБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ТСЦЄБтЛбЎў°±Л®µДГЬ¶ИУлЛщјУЛ®µДБїµД№ШПµИзНјЛщКѕЈ¬ПЦУРБтЛбУл°±Л®ёчТ»·ЭЈ¬ЗлёщѕЭ±нЦРРЕПўЈ¬»ШґрПВБРОКМвЈє
| ИЬЦКµДОпЦКµДБї ЕЁ¶И/molЎ¤LЈ1 | ИЬТєµДГЬ¶И/gЎ¤cmЈ3 |
БтЛб | c1 | ¦С1 |
°±Л® | c2 | ¦С2 |

ЈЁ1Ј©±нЦРБтЛбµДЦКБї·ЦКэОЄ________(І»РґµҐО»Ј¬УГє¬c1Ўў¦С1µДґъКэКЅ±нКѕ)ЎЈ
ЈЁ2Ј©ОпЦКµДБїЕЁ¶ИОЄc1 molЎ¤LЈ1µДБтЛбУлЛ®µИМе»э»мєП(»мєПєуИЬТєµДМе»э±д»ЇєцВФІ»јЖ)Ј¬ЛщµГИЬТєµДОпЦКµДБїЕЁ¶ИОЄ________ molЎ¤LЈ1ЎЈ
ЈЁ3Ј©Ѕ«ОпЦКµДБїЕЁ¶И·Ц±рОЄc2 molЎ¤LЈ1єН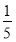 c2 molЎ¤LЈ1µД°±Л®µИЦКБї»мєПЈ¬ЛщµГИЬТєµДГЬ¶И________(МоЎ°ґуУЪЎ±ЎўЎ°РЎУЪЎ±»тЎ°µИУЪЎ±Ј¬ПВН¬)¦С2 gЎ¤cmЈ3Ј¬ЛщµГИЬТєµДОпЦКµДБїЕЁ¶И________
c2 molЎ¤LЈ1µД°±Л®µИЦКБї»мєПЈ¬ЛщµГИЬТєµДГЬ¶И________(МоЎ°ґуУЪЎ±ЎўЎ°РЎУЪЎ±»тЎ°µИУЪЎ±Ј¬ПВН¬)¦С2 gЎ¤cmЈ3Ј¬ЛщµГИЬТєµДОпЦКµДБїЕЁ¶И________ 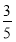 c2 molЎ¤LЈ1(Йи»мєПєуИЬТєµДМе»э±д»ЇєцВФІ»јЖ)ЎЈ
c2 molЎ¤LЈ1(Йи»мєПєуИЬТєµДМе»э±д»ЇєцВФІ»јЖ)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§¶юВЦЧЁМвН»ЖЖ ЧЁМвТ»ОпЦКµДЧйіЙРФЦКєН·ЦАаБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРёчЧйОпЦКµД·ЦАа¶јХэИ·µДКЗ(АЁєЕАпµДКЗАа±р)ЈЁ Ј©
AЈ®їХЖш(»мєПОп)ЎўC2H5OH(ґј)ЎўH2SO4(АлЧУ»ЇєПОп)ЎўCO2(·ЗµзЅвЦК)
BЈ®Тє°±(Зв»ЇОп)ЎўNH4Cl(п§СО)ЎўHNO3(є¬СхЛб)ЎўNaOH(ЗїµзЅвЦК)
CЈ®HCl(№ІјЫ»ЇєПОп)ЎўCH3COOH(фИЛб)ЎўNa2O2(јоРФСх»ЇОп)ЎўCH3I(В±ґъМю)
DЈ®NO2(ЛбРФСх»ЇОп)ЎўCH3CHO(УР»ъОп)ЎўCO(УР»ъОп)ЎўCH3COOCH3(хҐ)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв8µз»ЇС§ФАнБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
УГ¶иРФµзј«µзЅвNaClєНCuSO4»мєПТє250 mL,ѕ№эТ»¶ОК±јдєу,БЅј«ѕщµГµЅ11.2 LЖшМе(±кЧјЧґїцПВ),ФтПВБРУР№ШГиКцЦР,ХэИ·µДКЗЈЁ Ј©
A.Сфј«·ўЙъµД·ґУ¦Ц»УР:4OH--4e-=2H2O+O2 Ўь
B.БЅј«µГµЅµДЖшМеѕщОЄ»мєПЖшМе
C.ИфCu2+ЖрКјЕЁ¶ИОЄ1 molЎ¤L-1,Фтc(Cl-)ЖрКјОЄ 2 molЎ¤L-1
D.Cu2+µДЖрКјОпЦКµДБїУ¦ґуУЪ0.5 mol
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв7µзЅвЦКИЬТєБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
Ді»ЇС§С§П°РЎЧйОЄСРѕїHAЎўHBєНMOHµДЛбјоРФµДПа¶ФЗїИх,ЙијЖТФПВКµСй:іЈОВПВЅ«pH=2µДБЅЦЦЛбИЬТєHAЎўHBєНpH=12µДMOHјоИЬТєёч1 mL,·Ц±рјУЛ®ПЎКНµЅ1 000 mL,ЖдpHµД±д»ЇУлИЬТєМе»эµД№ШПµИзНј,ёщѕЭЛщёшµДКэѕЭ,Зл»ШґрПВБРОКМв:
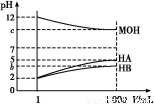
(1)HAОЄ Лб,HBОЄ Лб(МоЎ°ЗїЎ±»тЎ°ИхЎ±)ЎЈ
(2)Ифc=9,ФтПЎКНєуµДИэЦЦИЬТєЦР,УЙЛ®µзАлµДЗвАлЧУЕЁ¶ИµДґуРЎЛіРтОЄ (УГЛбЎўјо»ЇС§КЅ±нКѕ)ЎЈ
(3)Ифc=9,Ѕ«ПЎКНєуµДHAИЬТєєНMOHИЬТєИЎµИМе»э»мєП,ФтЛщµГИЬТєЦРc(A-)Улc(M+)µДґуРЎ№ШПµОЄc(A-) (МоЎ°ґуУЪЎ±ЎўЎ°РЎУЪЎ±»тЎ°µИУЪЎ±)c(M+)ЎЈ
(4)Ифb+c=14,ФтMOHОЄ јо(МоЎ°ЗїЎ±»тЎ°ИхЎ±)ЎЈЅ«ПЎКНєуµДHBИЬТєєНMOHИЬТєИЎµИМе»э»мєП,ЛщµГ»мєПИЬТєµДpH 7(МоЎ°ґуУЪЎ±ЎўЎ°РЎУЪЎ±»тЎ°µИУЪЎ±)ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв7µзЅвЦКИЬТєБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБРЛµ·ЁХэИ·µДКЗЈЁ Ј©
A.іЈОВПВґЧЛб·ЦЧУІ»їЙДЬґжФЪУЪpHЈѕ7µДјоРФИЬТєЦР
B.іЈОВПВПтВИ»Їп§ИЬТєЦРјУИлЙЩБї°±Л®К№ИЬТєµДpH=7,Фт»мєПИЬТєЦРc(N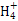 )Јѕc(Cl-)
)Јѕc(Cl-)
C.0.1 molЎ¤L-1µДВИ»Їп§ИЬТєУл0.05 molЎ¤L-1µДЗвСх»ЇДЖИЬТєµИМе»э»мєПєуИЬТєЦРАлЧУЕЁ¶ИµДґуРЎ№ШПµКЗ:c(Cl-)Јѕc(N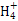 )Јѕc(Na+)Јѕc(OH-)Јѕc(H+)
)Јѕc(Na+)Јѕc(OH-)Јѕc(H+)
D.0.1 molЎ¤L-1Бт»ЇДЖИЬТєЦРАлЧУЕЁ¶ИµД№ШПµ:c(Na+)=c(S2-)+c(HS-)+c(H2S)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв6»ЇС§·ґУ¦ЛЩВКєН»ЇС§ЖЅєвБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
Ді№¤Тµ·ґУ¦ОЄ:X2(g)+3Y2(g) 2XY3(g)ЎЈНјўс±нКѕФЪТ»¶ЁОВ¶ИПВґЛ·ґУ¦№эіМЦРµДДЬБї±д»Ї;Нјўт±нКѕФЪ2 LµДГЬ±ХИЭЖчЦР·ґУ¦К±X2µДОпЦКµДБїЛжК±јдµД±д»ЇЗъПЯ;Нјўу±нКѕФЪЖдЛыМхјюІ»±дµДЗйїцПВ,ёД±дЖрКјОпY2µДОпЦКµДБї¶ФґЛ·ґУ¦ЖЅєвµДУ°ПмЎЈ
2XY3(g)ЎЈНјўс±нКѕФЪТ»¶ЁОВ¶ИПВґЛ·ґУ¦№эіМЦРµДДЬБї±д»Ї;Нјўт±нКѕФЪ2 LµДГЬ±ХИЭЖчЦР·ґУ¦К±X2µДОпЦКµДБїЛжК±јдµД±д»ЇЗъПЯ;Нјўу±нКѕФЪЖдЛыМхјюІ»±дµДЗйїцПВ,ёД±дЖрКјОпY2µДОпЦКµДБї¶ФґЛ·ґУ¦ЖЅєвµДУ°ПмЎЈ
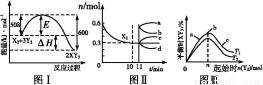
ПВБРЛµ·ЁХэИ·µДКЗЈЁ Ј©
A.УЙНјўсїЙЦЄ,јУИлККµ±µДґЯ»ЇјБ,EєН¦¤H¶јјхРЎ
B.НјўтЦР0Ў«10 minДЪёГ·ґУ¦µДЖЅѕщЛЩВКv(Y2)=0.045 molЎ¤L-1Ў¤min-1,ґУ11 minЖрЖдЛыМхјюІ»±д,С№ЛхИЭЖчµДМе»эОЄ1 L,Фтn(X2)µД±д»ЇЗъПЯОЄd
C.НјўуЦРaЎўbЎўcИэµгЛщґ¦µДЖЅєвЧґМ¬ЦР,·ґУ¦ОпX2µДЧЄ»ЇВКЧоёЯµДКЗbµг
D.НјўуЦРT1єНT2±нКѕОВ¶И,¶ФУ¦ОВ¶ИПВµДЖЅєвіЈКэОЄK1ЎўK2,ФтT1ЈјT2,K1ЈјK2
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв4»ЇС§·ґУ¦ЦРµДДЬБї±д»ЇБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ўс.АыУГ»ЇС§ФАнїЙТФ¶Ф№¤і§ЕЕ·ЕµД·ПЛ®Ўў·ПФьµИЅшРРУРР§јмІвУлєПАнґ¦АнЎЈУГТТП©ЧчОЄ»№ФјБЅ«µЄµДСх»ЇОп»№ФОЄN2КЗИјГєСМЖшµДТ»ЦЦНСПх(іэNOx)јјКхЎЈЖдНСПх»ъАнИзНјЛщКѕЎЈРґіцёГНСПх№эіМЦРТТП©єНNO2·ґУ¦µД»ЇС§·ЅіМКЅ ЎЈ
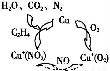
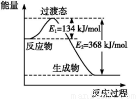
ўт.(1)ИзНјКЗ1 mol NO2(g)єН1 mol CO(g)·ґУ¦ЙъіЙCO2єНNO№эіМЦРµДДЬБї±д»ЇКѕТвНј,ИфФЪ·ґУ¦МеПµЦРјУИлґЯ»ЇјБ,·ґУ¦ЛЩВКФцґу,E1µД±д»ЇКЗ (МоЎ°ФцґуЎ±ЎўЎ°јхРЎЎ±»тЎ°І»±дЎ±,ПВН¬),¦¤HµД±д»ЇКЗ ЎЈ
(2)јЧґјЦКЧУЅ»»»Д¤ИјБПµзіШЦРЅ«јЧґјХфЖшЧЄ»ЇОЄЗвЖшµДБЅЦЦ·ґУ¦ФАнКЗўЩCH3OH(g)+H2O(g)=CO2(g)+3H2(g)¦¤H=+49.0 kJЎ¤mol-1;
ўЪCH3OH(g)+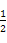 O2(g)=CO2(g)+2H2(g)¦¤H=-192.9 kJЎ¤mol-1ЎЈ
O2(g)=CO2(g)+2H2(g)¦¤H=-192.9 kJЎ¤mol-1ЎЈ
УЦЦЄўЫH2O(g)=H2O(l) ¦¤H=-44 kJЎ¤mol-1ЎЈ
ФтјЧґјХфЖшНкИ«ИјЙХЙъіЙТєМ¬Л®µДИИ»ЇС§·ЅіМКЅОЄ ЎЈ
РґіцјЧґјЦКЧУЅ»»»Д¤ИјБПµзіШФЪЛбРФМхјюПВµДёєј«·ґУ¦КЅ: ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ёЯїј»ЇС§ЧЁМвН»ЖЖСµБ· ЧЁМв1ОпЦКµДЧйіЙРФЦК·ЦАаєН»ЇС§УГУпБ·П°ѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
·ЦАа·ЁФЪ»ЇС§С§їЖµД·ўХ№ЦРЖрµЅЦШТЄЧчУГЎЈПВБР·ЦАа±кЧјєПАнµДКЗЈЁ Ј©
A.ёщѕЭ·ЦЙўПµµДОИ¶ЁРФґуРЎЅ«Жд·ЦОЄИЬТєЎўЅєМеєНЧЗТє
B.ёщѕЭ·ґУ¦µДИИР§У¦Ѕ«»ЇС§·ґУ¦·ЦОЄ·ЕИИ·ґУ¦єНОьИИ·ґУ¦
C.ёщѕЭИЬТєµјµзДЬБ¦µДЗїИх,Ѕ«µзЅвЦК·ЦОЄЗїµзЅвЦКєНИхµзЅвЦК
D.ёщѕЭФЄЛШФЧУЧоНвІгµзЧУКэµД¶аЙЩЅ«ФЄЛШ·ЦОЄЅрКфФЄЛШєН·ЗЅрКфФЄЛШ
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com