
| A. | 加热 | B. | 滴入数滴硫酸铜溶液 | ||
| C. | 加入少量NaCl溶液 | D. | 加入少量KNO3溶液 |
分析 加快反应速率,可以采用升高温度或增大反应物浓度等方法,但不影响生成物氢气的总量,说明锌不和其它物质反应而影响生成氢气,以此解答该题.
解答 解:A.加热,升高温度,可增大活化分子百分数,增大反应速率,不影响生成氢气的总量,故A正确;
B.加入几滴硫酸铜溶液,锌置换出铜,形成原电池反应,增大反应速率,但消耗锌,生成氢气的总量减少,故B错误;
C.加入氯化钠溶液,浓度减小,反应速率减小,故C错误;
D.硝酸根离子在酸性条件下具有强氧化性,与锌反应不生成氢气,故D错误.
故选A.
点评 本题考查化学反应速率影响因素,为高频考点,注意题干中要求“加快反应速率但不影响氢气总量”是解本题关键,易错选项是D注意硝酸和锌反应不生成氢气,为易错点.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
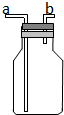 如图所示的装置在实验室种用途比较广泛.
如图所示的装置在实验室种用途比较广泛.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
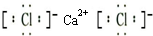 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol NH4+含有的电子数为1.1NA | |
| B. | NH4+中N元素的化合价为-3,在氧化还原反应中常作氧化剂 | |
| C. | 0.1 L 3 mol•L-1的NH4NO3溶液中氮原子数等于0.6NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)>c(NO3-) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1 mol/L Na2CO3溶液:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HA是一种强酸 | B. | 反应后溶液中c(OH-)<c(H+) | ||
| C. | c(A-)>c(B+)>c(H+)>c(OH-) | D. | 反应后混合溶液中还含有HA分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com