
I、某化学兴趣小组利用以下装置模拟合成氨并制备少量氨水
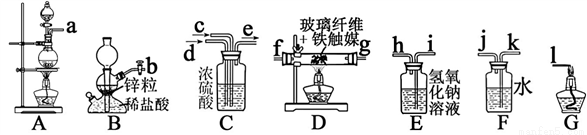
已知:加热(85℃)NH4Cl和NaNO2饱和溶液可以制取N2
B中仪器名称是___________________;
⑵为了完成实验,装置从左到右接口的连接顺序是_____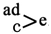 ______;
______;
⑶D中玻璃纤维的作用是_________________;
⑷小组中甲同学认为F装置不太合理,实验中会产生倒吸。乙同学认真分析后认为该装置无需改进,他的理由是________________________;
II、实验探究
⑸该小组同学利用制备的氨水再进行银镜反应实验。经查阅资料,配制的银氨溶液主要成分是[Ag(NH3)2]OH,小组同学对其组成进行了如下实验探究:
①在洁净的小试管中加入2mL 2%的AgNO3溶液,然后边振荡试管边滴加2%的稀氨水溶液,至最初产生的沉淀恰好溶解为止,制得银氨溶液。
②在制得的银氨溶液中加入无水乙醇,溶液变浑浊,过滤,用__________洗涤,得到白色固体;
③将该白色固体用适量蒸馏水溶解,得到无色溶液,用广范pH试纸检验溶液近似呈中性;向溶液中逐滴加入稀盐酸至不再产生沉淀,静置,取上层清液于另一支放有一小片铜的小试管中并微热,发现铜片的表面有气泡产生,遇到空气变成红棕色;另取少量上层清液加过量的NaOH溶液并加热,得到无色刺激性气体。由此确定通过上述方法制备的白色固体主要成分是___________________;
⑹请根据以上探究,设计实验来制备少量纯净的[Ag(NH3)2]OH溶液:取2mL 2%的AgNO3溶液于洁净的小试管中,_________________,即得到[Ag(NH3)2]OH溶液。
科目:高中化学 来源:2016-2017学年北京市怀柔区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列化学反应方程式中,不能用离子方程式Ba2++SO42-=BaSO 4↓表示的是( )
4↓表示的是( )
A.Ba(NO3)2+H2SO4= BaSO4↓+2HNO3 B.BaCl2+Na2SO4=BaSO4↓+2NaCl
C.BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ D.BaCl2+H2SO4= BaSO4↓+2HCl
查看答案和解析>>
科目:高中化学 来源:湖北省沙市2016-2017学年高二下学期第三次双周考化学试卷(A卷) 题型:填空题
人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,再利用电解法使K2CO3 溶液再生,其装置示意图如下:
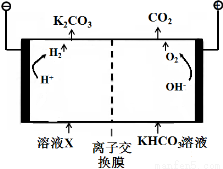
在阳极区发生的反应包括 和H ++ HCO3- = H2O + CO2↑。
简述CO32-在阴极区再生的原理 。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。
已知:25 ℃,101 KPa下: H2(g) + 1/2 O2(g) === H2O(g) Δ H1= -242 kJ/mol
CH3OH(g) + 3/2 O2(g) === CO2 (g) + 2 H2O(g) Δ H2= -676 kJ/mol
① 写出CO2和H2生成气态甲醇等产物的热化学方程式 。
② 下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
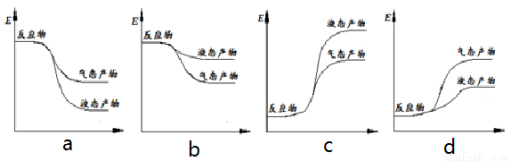
(3)在密闭的再生装置中,加入5 mol H2与2 mol CO2发生反应生成甲醇,反应达到平衡时,改变温度(T)和压强(P),反应混合物中甲醇(CH3OH)的物质的量分数变化情况如下图所示,下列说法正确的是

A.P1> P2> P3>P4
B.甲醇的物质的量分数越高,反应的平衡常数越大
C.图示中,该反应的温度变化为:T1> T2> T3>T4
D.T4、P4、时,H2的平衡转化率为60%
(4)已知某种甲醇燃料电池中,电解质溶液为酸性,示意图如下:
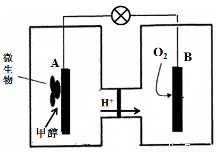
工作结束后,B电极室溶液的pH与工作前相比将 (填写“增大”、“减小”或“不变”,溶液体积变化忽略不计)。A电极附近甲醇发生的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:湖北省沙市2016-2017学年高二下学期第三次双周考化学试卷(A卷) 题型:选择题
下列对分子及其性质的解释中,不正确的是( )
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子
C. 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子而HClO为0
D. 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物
查看答案和解析>>
科目:高中化学 来源:湖北省沙市2016-2017学年高二下学期第三次双周考化学试卷(A卷) 题型:选择题
“防晒霜”之所以能有效地减轻紫外光对人体的伤害,是因为它所含的有效成分的分子中有π键,如氨基苯甲酸、羟基丙酮等。这些有效成分分子中的π电子可在吸收紫外光后被激发,从而阻挡部分紫外光对皮肤的伤害。下列分子中不含有π键的是( )
A. 乙炔分子 B. 乙烷分子 C. 氮气分子 D. 乙烯分子
查看答案和解析>>
科目:高中化学 来源:2017届湖北省、襄阳五中、襄阳四中等)高三下学期第二次联考理综化学试卷(解析版) 题型:选择题
设NA表示阿伏伽德罗常数的值。下列说法正确的是( )
A. 向含有FeI2的溶液中通入适量氯气,当有1molFe2+被氧化时,该反应转移电子数目为3NA
B. 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5 NA
C. 含0.1molNH4HSO4的溶液中,阳离子数目略小于0.2NA
D. C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代,1mol此有机物所含共用电子对数目为13NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省达州市年高二上学期期末检测化学试卷(解析版) 题型:选择题
在10L定容密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2。下列分析不正确的是
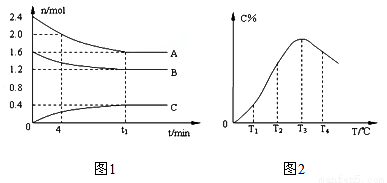
A. t1时刻前,混合气体的密度减小,t1时刻后,混合气体的密度不变
B. 该反应的平衡常数表达式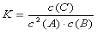
C. 由T1向T2变化时,V正> V逆
D. 此反应的正反应为放热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省达州市年高二上学期期末检测化学试卷(解析版) 题型:选择题
下列有关叙述或化学用语表示正确的是
A. S2-的结构示意图: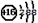 B. 过氧化氢的电子式:
B. 过氧化氢的电子式: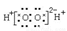
C. Ge原子的简化电子排布式:[Ar]4s24p2 D. 氯化钠的分子式:NaCl
查看答案和解析>>
科目:高中化学 来源:福建省2016-2017学年高一3月月考化学试卷 题型:选择题
运用元素周期律分析下面的推断,其中错误的是:①铍(Be)的氧化物的水化物可能具有两性,②铊(Tl)既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气,③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸,④锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱,⑤硫酸锶(SrSO4)是难溶于水的白色固体,⑥硒化氢(H2Se)是无色,有毒,比H2S稳定的气体( )
A. ①②③④ B. ②④⑥ C. ①③⑤ D. ②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com