
| A. | 巴豆酸的官能团是:碳碳双键、羧基 | |
| B. | 纯碱溶液、溴水、乙醇、酸高锰酸钾溶液均可与巴豆酸反应 | |
| C. | 巴豆酸的化学式为C4H6O | |
| D. | 巴豆酸与丁酸互为同分异构体 |
分析 A.由巴豆酸的结构可知,巴豆酸含有碳碳双键与羧基;
B.巴豆酸含有碳碳双键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化反应;
C.根据结构简式确定分子式;
D.巴豆酸与丁酸的分子式不相同.
解答 解:A.由巴豆酸的结构可知,巴豆酸含有官能团有:碳碳双键与羧基,故A正确;
B.巴豆酸含有羧基,能与纯碱反应产生二氧化碳,能与乙醇发生酯化反应,含有碳碳双键,能与溴水发生加成反应,能被酸性高锰酸钾溶液氧化,故B正确;
C.根据结构简式可知,巴豆酸化学式为C4H6O,故C正确;
D.巴豆酸分子式为C4H6O,丁酸的分子式为C4H8O,二者分子式不相同,不是同分异构体,故D错误,
故选BC.
点评 本题考查有机物的结构与性质,侧重对基础知识的巩固,注意掌握官能团的性质,难度不大.


 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 12C和14C互为同位素 | |
| B. | (CH3)2CHCH2CH3与CH3C(CH3)3互为同分异构体 | |
| C. | 冰和干冰互为同素异形体 | |
| D. | 乙醇(CH3CH2OH)与二甲醚(CH3-O-CH3)互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中的压强不再发生变化 | |
| B. | X、Y、Z的物质的量之比为1:2:2 | |
| C. | X、Y、Z的速率之比1:2:2 | |
| D. | 单位时间内生成n mol Z,同时消耗n mol Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、SO2、BF2、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构 | |
| B. | CCl4和NH3都是以极性键结合的极性分子,P4和NO2都是共价化合物 | |
| C. | 在CaO和SiO2晶体中,都不存在单个小分子 | |
| D. | π键是由两个p电子“头碰头”重叠形成,σ键是镜面对称,而π键是轴对称 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
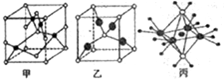
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| B. | 将标准状况下1.12L氯气通入10mL 1mol•L-1的溴化亚铁溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | |
| C. | 氢氧化铁溶于氢碘酸溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O | |
| D. | 4mol•L-1的NaAlO2溶液和7mol•L-1的盐酸等体积混合:AlO2-+4H+=Al3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com