
【题目】在烷烃分子中的基团:CH3、CH2、![]() 、
、![]() 中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用nl、n2、n3、n4表示。
中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用nl、n2、n3、n4表示。
例如: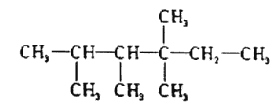 分子中,nl=6,n2=1,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
分子中,nl=6,n2=1,n3=2,n4=1。在烷烃(除甲烷外)分子中,各种类型的原子个数之间存在着一定的关系。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子数为A,A与nl、n2、n3、n4的关系是:A=_________,或A=_________。
(2)四种碳原子数之间的关系为nl=____________。
(3)若某分子中n2=n3=n4=1,写出该分子的结构简式和键线式,并对其进行命名:___________。
【答案】(1)3n1+2n2+n3,2(n1+n2+n3+n4)+2;(2)n3+2n4+2;
(3) ;2,2,3-三甲基戊烷;
;2,2,3-三甲基戊烷;
 ;2,3,3-三甲基戊烷;
;2,3,3-三甲基戊烷;
 ;2,2,4-三甲基戊烷。
;2,2,4-三甲基戊烷。
【解析】
试题分析:(1)因为伯、仲、叔、季碳原子结合的H原子分别为3、2、1、0个,所以根据伯、仲、叔碳原子数即可确定烷烃分子中H原子数为3n1+2n2+n3;根据烷烃的分子通式为CnH2n+2,n=n1+n2+n3+n4,即可确定烷烃分子中的H原子数为2(n1+n2+n3+n4)+2。
(2)由(1)中H原子数的关系可得3n1+2n2+n3=2(n1+n2+n3+n4)+2,整理即得n1=n3+2n4+2。
(3)分子中n2=n3=n4=1,则符合条件的分子的结构简式和键线式及命名分别为:
 ;2,2,3-三甲基戊烷;
;2,2,3-三甲基戊烷;
 ;2,3,3-三甲基戊烷;
;2,3,3-三甲基戊烷;
 ;2,2,4-三甲基戊烷。
;2,2,4-三甲基戊烷。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种物质有如下相互转化关系(其中各X、W为单质,Y、Z为化合物,未列出反应条件)。
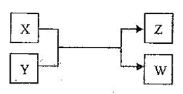
Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
工业上Z有多种用途,用化学方程式表示Z的一种用途:________________。
生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到一种碘酸盐,此反应的离子方程式是________________。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是________________。
(2)若用下列装置只进行Z+W→X+Y反应(夹持装置未画出);
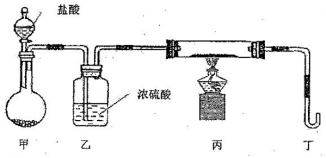
①完成此实验有多步操作,其中三步是:
A.点燃酒精灯 B.滴加盐酸 C.检验气体纯度
这三步操作的先后顺序是 (填字母)。
②为保证实验成功,上述装置需要改进,方法是(用文字叙述) 。
(3)将3.38gZ加入50ml4mol/L 稀HNO3中充分反应,产生112ml的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀。当沉淀量最多时,至少需要加入2mol/L的NaOH溶液__________ml.(精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于海水资源的说法不正确的是( )
A. 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B. 从海水中可以提取铀和重水等核原料
C. 海水中的溴、氟等元素均为微量元素,但仍有提取的价值
D. 海水中金的储存量约为陆地的170倍,但它的富集程度却很低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人生病时要合理用药.下列药品与其作用匹配的是( )
A.氢氧化铝:中和过多胃酸 B.阿司匹林:消炎抗菌
C.青霉素:解热镇痛 D.医用碘酒:人体补碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水垢成分之一的氢氧化镁溶于稀盐酸的离子方程式书写正确的是
A. Mg(OH)2+H+ = Mg2++H2O B. Mg(OH)2+HCl=Mg2++H2O+Cl-
C. Mg(OH)2+2H+ = Mg2++2H2O D. OH-+ H+ = H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.取1.43g Na2CO3·XH2O 溶于水配成10ml 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0ml,并收集到112ml CO2(标况)。
(1)稀盐酸物质的量浓度为____________。
(2)Na2CO3·xH2O的摩尔质量为_______________。
(3)x=___________。
Ⅱ.在智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,化学方程式是:
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(1)用“双线桥”标出电子转移的方向和数目。
(2)反应产物中,氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是SO2和H2S)的转化对环境保护具有重要意义。
(1)SO2的大量排放会引起严重的环境问题是 ,潮湿条件下,写出大气中SO2转化为HSO3-的方程式
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:
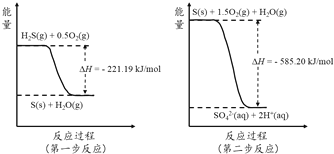
1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为
(3)SO2时工业制硫酸的原料之一,一定温度下,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g),过程中测定的部分数据见下表:
2SO3(g),过程中测定的部分数据见下表:
时间/min | n(SO2)/mol | n(O2)/mol |
0 | 0.10 | 0.050 |
4 | 0.050 | 0.025 |
5 | 0.040 | |
8 | 0.020 |
①反应在0-4min内的平均速率为v(SO2)= ;
②此温度下该反应的化学平衡常数K= 。
③8min时,维持温度不变,往反应容器中再通入0.020molSO2(g),0.010molO2(g),重新达到平衡时混合气体中SO2的百分含量将 (填“减小”、“增大”或“不变”。)
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化入右图所示:
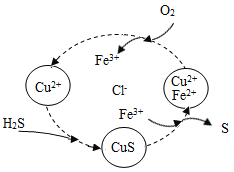
①在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有 。
②一般来说,如果一个反应的平衡常数大于105,通常认为反应进行得较安全;相反,如果一个反应的平衡常数夏普与10-5,则认为这个反应很难进行。
已知常温下各物质的溶度积及电离平衡常数:
CuS:Ksp=6.3×10-36;H2S:Ka1=1.3×10-7,Ka2=7.1×10-15,
通过计算说明反应CuS(s)+2H+(aq)=Cu2+(aq)+H2S(aq)进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
A. O2和O3互为同位素
B. O2和O3的相互转化是物理变化
C. 等物质的量的O2和O3含有相同的质子数
D. 在相同的温度与压强下,等体积的O2和O3含有相同的分子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com