
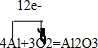 ,红墨水柱右端上升说明这是一个放热反应.
,红墨水柱右端上升说明这是一个放热反应.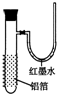
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:实验题
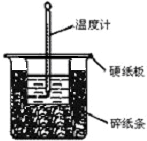 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 温度 序号 | 起始温度t1/℃ | 终止温度 T2/℃ | 温度差 △t/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25 | 25 | 27.3 | ||
| 2 | 25 | 25 | 27.4 | ||
| 3 | 25 | 25 | 28.6 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②③④ | C. | ③④⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有七个周期,十八个族 | B. | 是元素周期律的具体表现形式 | ||
| C. | 对工农业生产有一定的指导作用 | D. | 是学习和研究化学的重要工具 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向澄清石灰水中加入盐酸 Ca(OH)2+2H+→Ca2++2H2O | |
| B. | 硫化亚铁与盐酸反应 S2-+2H+→H2S↑ | |
| C. | 氯化铝溶液与过量氨水反应 Al3++3NH3•H2O→Al(OH)3↓+3NH4+ | |
| D. | 氯化亚铁溶液中通入少量氯气 Fe2++Cl2→Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属钠着火可用水扑灭 | |
| B. | 将几滴FeCl3饱和溶液滴入氢氧化钠溶液可制备Fe(OH)3胶体 | |
| C. | 向含有等量NaI、NaCl的溶液中逐滴加入AgNO3溶液,先产生浅黄色沉淀 | |
| D. | 用浓氢氧化钠溶液和湿润红色石蕊试纸检验某溶液中是否有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
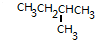 ,则该烃所有可能的结构简式为
,则该烃所有可能的结构简式为 或
或 ;
; .
. 或
或 .
. ,如果要合成
,如果要合成 所用的原始原料可以是AC
所用的原始原料可以是AC查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com