
反应m A+n B⇌p C在某温度下达到平衡.
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是 .
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向 方向移动.
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为 态.
考点:
化学平衡的影响因素;化学平衡状态的判断.
专题:
化学平衡专题.
分析:
①根据影响化学平衡因素结合速率大小分析判断反应前后的体积变化;
②反应前后系数相同,改变压强平衡移动说明反应物中含有固体或纯液体;
③固体和纯液体对平衡无影响.
解答:
解:①反应mA+nB⇌pC,若A、B、C都是气体,减压后正反应速率小于逆反应速率,证明逆向反应是气体体积增大的反应,得到m+n>p,
故答案为:m+n>p;
②若反应mA+nB⇌pC;C为气体,且m+n=p,在加压时化学平衡发生移动,说明AB中至少有一种是固体或纯液体,加压平衡逆向进行,
故答案为:逆向;
③若反应mA+nB⇌pC;如果在体系中增加或减少B的量,平衡均不发生移动,证明B一定是固体或纯液体,不是气体,
故答案为:气.
点评:
本题考查了化学平衡的影响因素判断,主要考查压强对平衡的影响和物质性质的判断,化学平衡的移动规律是解题的关键.


科目:高中化学 来源: 题型:
铁屑溶于过量的稀硫酸,过滤后向滤液中加入足量硝酸,再加入过量的氨水,有沉淀生成.过滤,加热沉淀物至质量不再发生变化,得到残渣.上述沉淀和残渣分别为( )
|
| A. | Fe(OH)3;Fe2O3 | B. | Fe (OH)2;FeO |
|
| C. | Fe (OH)2、Fe(OH)3;Fe3O4 | D. | Fe2O3;Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式书写正确的是( )
|
| A. | NaHCO3=Na++H++CO32﹣ | B. | HF⇌H++F﹣ |
|
| C. | H2CO3⇌2H++CO32﹣ | D. | CH3COONH4⇌CH3COO﹣+NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于3Fe(s)+4H2O(g)⇌Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
|
| A. | K= |
|
| B. | K= |
|
| C. | K= |
|
| D. | K= |
查看答案和解析>>
科目:高中化学 来源: 题型:
今有①盐酸、②醋酸、③硫酸三种稀溶液,用序号回答下列问题.
(1)若三种酸的物质的量浓度相等.
a.三种溶液中的c(H+)大小关系为 .
b.取等体积上述三种溶液,分别用同浓度的NaOH溶液完全中和,所需NaOH体积大小关系为 .
(2)若三种酸溶液中的c(H+)相等.
a.三种酸的物质的量浓度大小关系为 .
b.取等体积上述三种溶液,分别用同浓度的NaOH溶液完全中和,所需NaOH溶液体积大小关系为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是( )


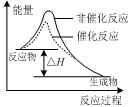
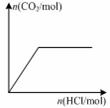
图甲 图乙 图丙 图丁
A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B.图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变
D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种叙述中,正确的是 ( )
①Cl-和Cl2的性质相同;②ClO3-具有氧化性;③Cl-比Cl多一个电子;④Cl-具有酸性; ⑤盐酸兼有酸性、氧化性、还原性; ⑥Cl2的氧化性比盐酸的强;⑦Cl2只有氧化性而没有还原性
A.①②⑤⑥ B. ①②④⑥
C. ②③⑤⑥ D. ②③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
COCl2(g)  CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
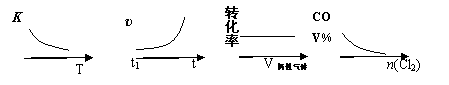
① ② ③ ④
A.①表示随温度升高,平衡常数的变化
B.②表示加入催化剂,反应速率随时间的变化
C.③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D.④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com