
【题目】某浓度稀HNO3与金属M反应时,能得到+2价硝酸盐,反应时M与HNO3的物质的量之比为5 ∶12,则反应时HNO3的还原产物是 ( )
A. NH4NO3B. N2C. N2OD. NO
科目:高中化学 来源: 题型:
【题目】在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3 , 溶质的质量分数为w,溶质的物质的量浓度为c mol/L.下列叙述中正确的是( )
①w= ![]() ×100%
×100%
②c= ![]()
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w.
A.①③
B.②③
C.①②
D.只有②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中制取高纯碳酸钴(CoCO3)的工艺流程如下:
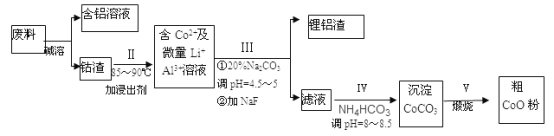
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为_________________________。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的离子反应方程
式为_____________________(产物中只有一种酸根)。也可用H2SO4和H2O2代替H2SO4、Na2S2O3,那么该反应的化学方程式为______________;但若用HC1代替H2SO4会造成的后果是______________。
(3)过程Ⅲ中碳酸钠溶液的作用是沉淀Al3+和Li+,写出沉淀Al3+的离子方程式___________________。
(4)过程Ⅳ沉钴的离子方程式是______________________。
(5)CoCO3可用于制备锂离子电池的正极材料LiCoO2,其生产工艺是将n(Li):n(Co)=l:l的LiCO3和CoCO3的固体混合物在空气中加热至700℃~900℃。试写出该反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组,欲在常温常压下,用一定质量的铜镁合金与足量稀盐酸反应,利用图装置,测定样品中铜的质量分数. 
(1)实验反应原理:写出A中发生反应的离子方程式 .
(2)仪器识别:写出上图中仪器①的名称 .
(3)实验中,该兴趣小组同学测得以下数据
a.反应前样品铜镁合金的质量,记为m1 g
b.反应结束后,经过处理后的残余固体的质量,记为m2 g
c.经过一系列正确的操作后,读取量筒中的水的体积,记为V mL
d.查阅资料,常温常压下,H2的密度为ρ g/L
四位同学分成甲、乙两个小组,甲组同学利用重量法为思路,请合理选择以上数据,列式求铜的质量分数:×100%;乙组同学利用排水法测量气体体积为思路,请合理选择以上数据,列式求铜的质量分数:×100%
(4)误差分析环节中指导教师提出,甲、乙两组同学的思路中,会有很多因素导致测得的铜的质量分数出现误差,现将可能导致误差的因素罗列如下,回答相关问题:
a.读取量筒中水的体积时,未等装置中气体恢复至室温
b.未考虑B、C装置间连接导管中残留的水
c.未对反应后剩余的残余物进行洗涤
d.未对反应中挥发出的HCl气体进行除杂处理
导致铜的质量分数大于理论值的原因可能是(填符号)
导致铜的质量分数小于理论值的原因可能是(填符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沼气是一种能源,它的主要成分是CH4 . 0.5mol CH4完全燃烧生成CO2和H2O(l),放出445kJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H═+890 kJmol﹣1
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═+890 kJmol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═﹣890 kJmol﹣1
D.![]() CH4(g)+O2(g)═
CH4(g)+O2(g)═ ![]() CO2(g)+H2O(l)△H═﹣890 kJmol﹣1
CO2(g)+H2O(l)△H═﹣890 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1.E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2﹣相同. 
试回答:
(1)元素E在元素周期表中的位置是 .
(2)与元素D离子所含电子数和质子数均相同的微粒是 . (用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的为 . 若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:Ⅰ , Ⅱ , 观察到的实验现象是 .
(4)由以上五种元素组成的中学常见的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A,C,D的盐 |
b | C,D组成的化合物,且原子数之比为1:1 |
c | 化学组成为AC2 |
①a含有的化学键有;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列饮食搭配,最为均衡合理的是( )
A. 炖牛肉、炒白菜、红烧豆腐、西红柿蛋汤、馒头
B. 凉拌青菜、土豆丝、馒头
C. 糖醋排骨、清蒸鲤鱼、米饭
D. 油炸豆腐、红烧肉、鸡肉、米饭
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com