
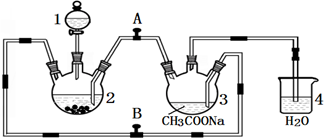
| 实际量 |
| 理论量 |
| 6.34g |
| 158.5g/mol |
| 1 |
| 2 |
| 5.64g |
| 7.52g |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
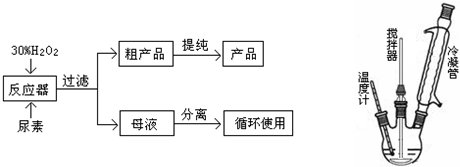
| 分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
| CO(NH2)2?H2O2 | 白色晶体 | 45℃ | 75-85℃ | 500g?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
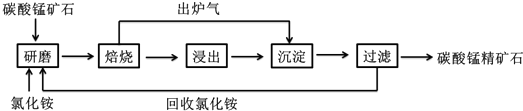
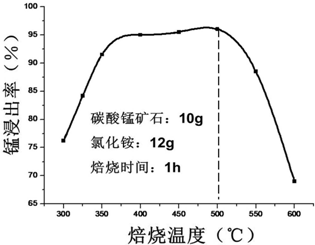
查看答案和解析>>
科目:高中化学 来源: 题型:
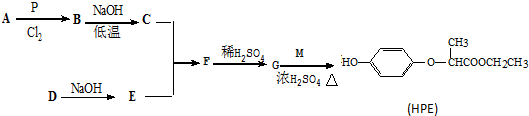
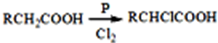
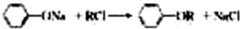
查看答案和解析>>
科目:高中化学 来源: 题型:
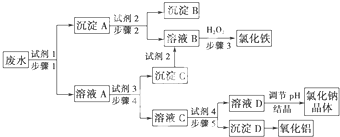
查看答案和解析>>
科目:高中化学 来源: 题型:
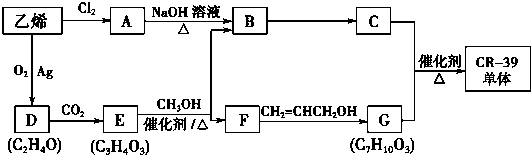
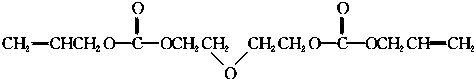
| 催化剂 |
| △ |
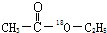 的合成路线,合成路线流程图示例如下:CH2-CH2
的合成路线,合成路线流程图示例如下:CH2-CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、AlO2─、Cl─ |
| B、Al3+、NH4+、CO32-、Cl─ |
| C、K+、Na+、ClO─、SO32─ |
| D、Na+、Ba2+、OH─、NO3─ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com