
分析 根据盖斯定律求出4CO(g)+2NO2(g)=N2(g)+4CO2(g)的反应热,反应中4.48L CO即0.2mol转移0.4mol电子,根据物质的量之比等于热量比求出放出的热量.
解答 解:①CO(g)+NO2(g)=NO(g)+CO2(g)△H=-a KJ•mol-1(a>0)
②2CO(g)+2NO (g)=N2(g)+2CO2(g)△H=-b KJ•mol-1(b>0)
将方程式①×2+②得4CO(g)+2NO2(g)=N2(g)+4CO2(g)△H=(-a) KJ•mol-1×2+(-b KJ•mol-1)=-(2a+b)KJ•mol-1
所以其热化学反应方程式为:4CO(g)+2NO2(g)=N2(g)+4CO2(g)△H=-(2a+b)KJ•mol-1,
根据方程式知转移电子的物质的量=$\frac{4.48L}{22.4L/mol}$×2=0.4mol,放出的热量=$\frac{4.48L}{22.4L/mol}$×$\frac{(2a+b)kJ/mol}{4}$=$\frac{(2a+b)}{20}$kJ,
故答案为:0.4mol;$\frac{(2a+b)}{20}$.
点评 本题考查了知转移电子数及其盖斯定律的有关计算,会利用盖斯定律书写出反应物之间的关系式是解本题关键,难度中等.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种难溶电解质,Ksp小的溶解度一定小 | |
| B. | 0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中c(Cl-)=c(I-) | |
| C. | 在硫酸钡的沉淀溶解平衡体系中加入蒸馏水,硫酸钡的Ksp增大 | |
| D. | 用锌片作阳极,铁片作阴极,电解ZnCl2溶液,铁片表面出现一层锌 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:
Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰色反应 | B. | 氧化性 | C. | 还原性 | D. | 不稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
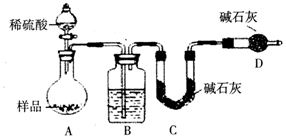
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com