
下列对于生活垃圾中生物质能的利用不合理的是( )
A.将生活垃圾进行处理后焚烧,利用产生的热能发电
B.将生活垃圾进行生物化学转换制得CH4
C.将生活垃圾拉到农村找个地方掩埋
D.让生活垃圾在一定条件下发生化学反应,产生热值较高的可燃气体
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
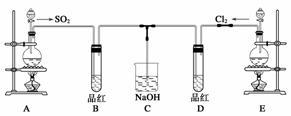
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是________________________________________________
(2)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)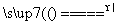 MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子总数为_______________________;
MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子总数为_______________________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:____________________________________,D:______________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)分析下列物质的物理性质,判断其晶体类型。
A.碳化铝,黄色晶体,熔点2200 ℃,熔融态不导电________;
B.溴化铝,无色晶体,熔点98 ℃,熔融态不导电________;
C.五氟化钒,无色晶体,熔点19.5 ℃,易溶于乙醇、氯仿、丙酮中________;
D.溴化钾,无色晶体,熔融时或溶于水中都能导电________。
(2)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为________。

(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如上图所示。面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.电解水生成氢气与氧气时,电能转变成化学能
B.煤燃烧时化学能转变成热能等
C.绿色植物光合作用过程中太阳能转变成化学能
D.白炽灯工作时电能全部转化成光能
查看答案和解析>>
科目:高中化学 来源: 题型:
可再生能源是我国重要的能源资源,在满足能源需求、改善能源结构、减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术是实现节能减排的一项重要措施。下列有关分析不正确的是( )
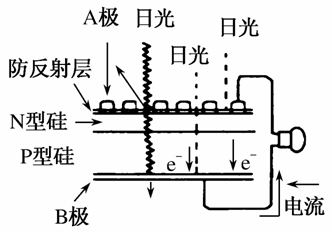
A.风能、太阳能属于可再生能源
B.推广可再生能源有利于经济可持续发展
C.上图是太阳能光伏发电原理图,图中A极为正极
D.光伏发电能量转化方式是太阳能直接转变为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法中,正确的是( )
A.葡萄糖是一种单糖
B.葡萄糖分子中有6个碳原子、6个水分子
C.常温下,葡萄糖可与新制的氢氧化铜悬浊液反应
D.1 mol葡萄糖完全燃烧需要9 mol氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烷、乙烯、乙炔共同具有的性质是( )
A.都能使溴水和酸性高锰酸钾溶液褪色
B.都能发生加聚反应生成高分子化合物
C.都不溶于水,且密度比水小
D.分子中各原子都处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
羟基磷灰石是一种重要的生物无机材料,其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:在剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
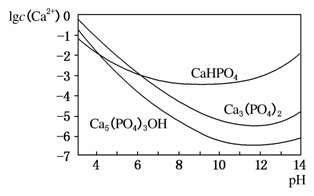
3种钙盐的溶解度随溶液pH的变化如图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O===Ca5(PO4)3OH↓+________+________。
②5Ca(OH)2+3H3PO4===______________________________。
(2)与方法A相比,方法B的优点是_______________________。
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是_______________________________________________。
(4)图中所示3种钙盐在人体中最稳定的存在形式是________________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com