
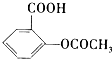
 )是常用的解热镇痛药.它遇水会缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为
)是常用的解热镇痛药.它遇水会缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为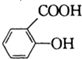 .
.分析 (1)在人体内产生碱性物质的称为碱性食品;
(2)阿司匹林是解热镇痛药;邻羟基苯甲酸的结构简式为 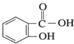 ,俗名为水杨酸;
,俗名为水杨酸;
(3)氢氧化铝与盐酸反应生成氯化铝和水.
解答 解:(1)产生碱性物质的称为碱性食品,如蔬菜、水果,茶叶等. 一般来说,大部分的蔬菜、水果都是碱性的,故答案为:碱;
(2)阿司匹林是解热镇痛药,水杨酸的结构简式: ,
,
故答案为:解热镇痛; ;
;
(3)氢氧化铝与盐酸反应生成氯化铝和水,离子反应为Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O.
点评 本题考查知识点较多,涉及化学与生活的联系、药物的主要成分和疗效,利用化学知识来解决生活中的问题即可解答,题目难度不大.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
| 分类、选项 | 酸 | 碱 | 盐 | 碱性氧化物 |
| A | H2SO4 | Na2CO3 | NaHCO3 | CaO |
| B | HCl | NH3•H2O | NaCl | Na2O |
| C | CO2 | Cu(OH)2 | MgCl2 | Na2O |
| D | HNO3 | KOH | CaO | CO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3+H2O═H2SO4 | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2Na+2H2O═2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气易液化,可储存于钢瓶中 | |
| B. | 实验室可以用向下排空气法收集氯气 | |
| C. | 氯气不能将碘化钾中的碘置换出来 | |
| D. | 氯气的摩尔质量为71g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
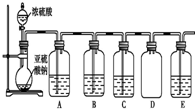 (1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.
(1)某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告.| 物质 | 类别 | 化学性 质预测 | 实验验证 | ||
| 实验操作 | 实验现象 | 实质(用离子 方程式表示) | |||
| 二氧 化硫 | 酸性 氧化物 | 与水 反应 | 将盛满SO2气体的试管倒立在水中,并测定试管中溶液的pH | ① | SO2+H2O ?H2SO3 |
| 与碱 反应 | ② | 出现白 色沉淀 | ③ | ||
| 装置 | 药品 | 作用 |
| A | 验证二氧化硫的还原性 | |
| B | ||
| C | 品红溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 | |
| C. | 实验室用排饱和食盐水的方法收集氯气 | |
| D. | 用铁触媒作催化剂加快化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com