
| A、体积:④<①<②<③ |
| B、密度:①<④<③<② |
| C、质量:④<①<③<② |
| D、氢原子数:②<④<③<① |
| 6.72L |
| 22.4L/mol |
| 3.01×1023 |
| 6.02×1023/mol |
| 13.6g |
| 34g/mol |
| M |
| Vm |
| 6.72L |
| 22.4L/mol |
| 3.01×1023 |
| 6.02×1023/mol |
| 13.6g |
| 34g/mol |
| M |
| Vm |


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
| 有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
| Ω | 1 | 2 | 1 | 4 |
| A、1molΩ=3的不饱和链烃再结合6molH 即达到饱和 |
| B、C10H8的Ω=7 |
| C、C4H8的不饱和度与C3H6、C2H4的不饱和度不相同 |
| D、CH3CH=CHCH3与环丁烷的不饱和度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
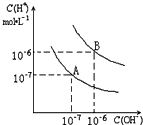 (1)实验测得:在室温下1L水中只有10-7mol的水电离,列式计算水的电离平衡常数KH2O;
(1)实验测得:在室温下1L水中只有10-7mol的水电离,列式计算水的电离平衡常数KH2O;查看答案和解析>>
科目:高中化学 来源: 题型:
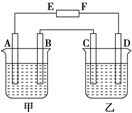 在如图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol?L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol?L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则
在如图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol?L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol?L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,3.0 g乙烷中含有的碳氢键数为0.7NA |
| B、将0.2 mol FeCl3水解制成胶体,所得胶体粒子数为 0.2NA |
| C、常温常压下,28 g的 C2H4和C3H6混合气体含有的原子数为 6NA |
| D、标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉、CuO、HClO、Cu |
| B、普通玻璃、H2O、Fe(SCN)3、葡萄糖 |
| C、水银、Na2O?CaO?6SiO2、BaSO4、SO3 |
| D、KAl(SO4)2?12H2O、KClO3、NH3?H2O、CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com