
”¾ĢāÄæ”æÓŠ»ś»Æ¹¤ŌĮĻ1,4-¶ž±½»ł-1,3-¶”¶žĻ©¼°Ä³æ¹½į³¦Ń×Ņ©ĪļÓŠŠ§³É·ÖµÄŗĻ³ÉĀ·ĻßČēĻĀ£Ø²æ·Ö·“Ó¦ĀŌČ„ŹŌ¼ĮŗĶĢõ¼ž£©£ŗ
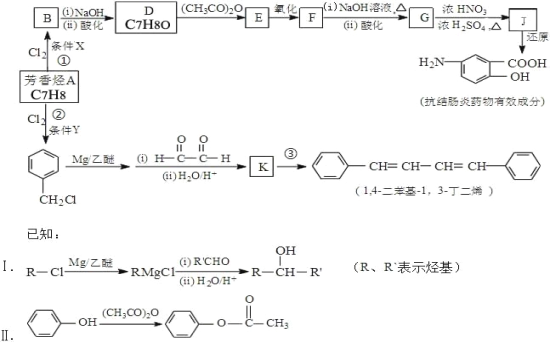
£Ø1£©æ¹½į³¦Ń×Ņ©ĪļÓŠŠ§³É·Ö·Ö×ÓÖŠµÄŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘŹĒ________”£
£Ø2£©¢ŚÖŠµÄ·“Ó¦Ģõ¼žŹĒ________£»GÉś³ÉJµÄ·“Ó¦ĄąŠĶŹĒ________”£
£Ø3£©¢ŁµÄ»Æѧ·½³ĢŹ½ŹĒ________”£
£Ø4£©FµÄ½į¹¹¼ņŹ½ŹĒ________”£
£Ø5£©¢ŪµÄ»Æѧ·½³ĢŹ½ŹĒ________”£
£Ø6£©Éč¼ĘD”śEŗĶF”śGĮ½²½·“Ó¦µÄÄæµÄŹĒ________”£
£Ø7£©1,4-¶ž±½»ł-1,3-¶”¶žĻ©ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Š“³ö·ūŗĻĻĀĮŠĢõ¼žµÄĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ_________”£
a£®½į¹¹ÖŠÓŠĮ½øö±½»·£¬ĪŽĘäĖü»·×“½į¹¹ b£®±½»·ÉĻµÄŅ»Ļõ»łČ”“ś²śĪļÓŠĮ½ÖÖ
”¾“š°ø”æōĒ»ł ōČ»ł¹āÕÕČ”“ś·“Ó¦![]()

 ±£»¤·ÓōĒ»ł£Ø·ĄÖ¹·ÓōĒ»ł±»Ńõ»Æ£©
±£»¤·ÓōĒ»ł£Ø·ĄÖ¹·ÓōĒ»ł±»Ńõ»Æ£©![]()
![]()
”¾½āĪö”æ
£Ø1£©øł¾Żæ¹½į³¦Ń×Ņ©ĪļÓŠŠ§³É·Ö·Ö×Ó½į¹¹¼ņŹ½£¬æÉÖŖĘäŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘŹĒōĒ»łŗĶōČ»ł£»ÕżČ·“š°ø£ŗōĒ»łŗĶōČ»ł”£
£Ø2£©¼×±½µÄ²ąĮ“Ā±“śµÄĢõ¼žÓėĶéĢžĻąĶ¬£¬¶¼ŹĒ¹āÕÕ£»GÉś³ÉJµÄ·“Ó¦Ģõ¼žŹĒÅØĻõĖį”¢ÅØĮņĖį”¢¼ÓČČ£¬ĖłŅŌ·“Ó¦ĄąŠĶŹĒČ”“ś·“Ó¦£»ÕżČ·“š°ø£ŗ¹āÕÕ£» Č”“ś·“Ó¦”£
£Ø3£©øł¾Żæ¹½į³¦Ń×Ņ©ĪļÓŠŠ§³É·Ö·Ö×ӵĽį¹¹¼ņŹ½ÅŠ¶Ļ£¬DĪŖĮŚ¼×±½·Ó£¬ĖłŅŌBĪŖĮŚĀČ¼×±½£¬¢ŁµÄ»Æѧ·½³ĢŹ½ŹĒ![]() £»ÕżČ·“š°ø£ŗ
£»ÕżČ·“š°ø£ŗ![]() ”£
ӣ
£Ø4£©øł¾ŻŅŃÖŖ¢ņµĆDµ½EÓ¦ŹĒ±£»¤·ÓōĒ»łµÄ·“Ó¦£¬Eµ½FŹĒ¼×»ł±»Ńõ»ÆµÄ·“Ó¦£¬ĖłŅŌFµÄ½į¹¹¼ņŹ½ĪŖ £»ÕżČ·“š°ø£ŗ
£»ÕżČ·“š°ø£ŗ ”£
ӣ
£Ø5£©ÓÉ1,4-¶ž±½»ł-1,3-¶”¶žĻ©µĆ½į¹¹¼ņŹ½¼°ŅŃÖŖ¢ńµÄ·“Ó¦·½³ĢŹ½ÅŠ¶Ļ¢Ū·¢ÉśĻūČ„·“Ó¦£¬»Æѧ·½³ĢŹ½ŹĒ£ŗ
 £»ÕżČ·“š°ø£ŗ
£»ÕżČ·“š°ø£ŗ
 ӣ
ӣ
£Ø6£©Dµ½E°Ń·ÓōĒ»ł×Ŗ»ÆĪŖõ„»ł£¬ÄæµÄŹĒ·ĄÖ¹Eµ½F²½ÖčÖŠ·ÓōĒ»ł±»Ńõ»Æ£¬Fµ½GÓÖ°Ńõ„»ł»¹ŌĪŖ·ÓōĒ»ł£¬ĖłŅŌÕūĢå×÷ÓĆŹĒ±£»¤·ÓōĒ»ł£Ø·ĄÖ¹·ÓōĒ»ł±»Ńõ»Æ£©£»ÕżČ·“š°ø£ŗ±£»¤·ÓōĒ»ł£Ø·ĄÖ¹·ÓōĒ»ł±»Ńõ»Æ£©”£
£Ø7£©øł¾ŻĢāÄæŅŖĒó1,4-¶ž±½»ł-1,3-¶”¶žĻ©µÄĶ¬·ÖŅģ¹¹ĢåÖŠµÄ±½»·ÉĻµÄŅ»Ļõ»łČ”“ś²śĪļÓŠĮ½ÖÖ£¬ 2øö±½»·ĖłĮ¬Č”“ś»łÓ¦ĶźČ«ĻąĶ¬£¬ĒŅ2øö±½»·ŹĒ¶Ō³Ę½į¹¹£¬ĖłŅŌæ¼ĀĒ1øö±½»·¼“æÉ£»±½»·ÉĻµÄŅ»Ļõ»łČ”“ś²śĪļÓŠĮ½ÖÖ£¬ĖµĆ÷Ćæøö±½»·ÉĻ¶¼ÓŠ¶ŌĪ»Č”“ś»ł£¬ĖłŅŌĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖ![]()
![]() £»ÕżČ·“š°ø
£»ÕżČ·“š°ø![]() ”¢
Ӣ![]() ӣ
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ŅŃÖŖ²ŻĖį£ØH2C2O4£©æÉŹ¹H2SO4Ėį»ÆµÄKMnO4ČÜŅŗĶŹÉ«£¬Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
¢ŁĒė²¹Č«²¢ÅäĘ½øĆ·“Ó¦·½³ĢŹ½£ŗ
_____H2C2O4+___KMnO4+___H2SO4 ”ś ___K2SO4+____ MnSO4+___ CO2”ü + ___H2O
¢ŚŌŚøĆ·“Ó¦»¹Ō²śĪļĪŖ________£ØŠ“»ÆѧŹ½£©
£Ø2£©Ä³ČÜŅŗÖŠæÉÄÜŗ¬ÓŠŅŌĻĀĄė×Ó£ŗNa+”¢K+”¢Fe3+”¢CO32£”¢SO42£”¢Cl££¬ĻÖ½ųŠŠČēĻĀŹµŃé£ŗ

øł¾ŻŹµŃéĻÖĻó»Ų“š£ŗ
øĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠµÄĄė×ÓŹĒ______________£»Ņ»¶Ø²»ŗ¬ÓŠµÄĄė×ÓŹĒ____________£»ĪŽ·ØČ·¶ØµÄĄė×ÓŹĒ____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNaClO2ŹĒŅ»ÖÖÖŲŅŖµÄɱ¾śĻū¶¾¼Į£¬Ņ²³£ÓĆĄ“ĘÆ°×ÖÆĪļµČ£¬ŅŃÖŖ£ŗNaClO2±„ŗĶČÜŅŗŌŚĪĀ¶ČµĶÓŚ38”ꏱĪö³ö¾§ĢåNaClO2![]() £¬ĪĀ¶ČøßÓŚ38”ꏱĪö³ö¾§ĢåNaClO2£¬ĪĀ¶ČøßÓŚ60”ꏱNaClO2·Ö½āÉś³ÉNaClO3ŗĶ
£¬ĪĀ¶ČøßÓŚ38”ꏱĪö³ö¾§ĢåNaClO2£¬ĪĀ¶ČøßÓŚ60”ꏱNaClO2·Ö½āÉś³ÉNaClO3ŗĶ![]() ”£ĘäŅ»ÖÖÉś²ś¹¤ŅÕČēĻĀ”£
”£ĘäŅ»ÖÖÉś²ś¹¤ŅÕČēĻĀ”£

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)NaClO2ÖŠ![]() µÄ»ÆŗĻ¼ŪĪŖ_____________”£
µÄ»ÆŗĻ¼ŪĪŖ_____________”£
(2)·“Ó¦I£ŗ
¢Ł![]() ×ö___________(Ģī”°Ńõ»Æ¼Į”±»ņ”°»¹Ō¼Į”±)”£
×ö___________(Ģī”°Ńõ»Æ¼Į”±»ņ”°»¹Ō¼Į”±)”£
¢Ś½«·“Ó¦IÖŠµÄ»Æѧ·½³ĢŹ½²¹³äĶźÕū£ŗ
![]() _____________
_____________
(3)µē½āII£ŗ
¢ŁĖłÓĆŹ³ŃĪĖ®ÓÉ“ÖŃĪĖ®¾«Öʶų³É£¬¾«ÖĘŹ±£¬ĪŖ³żČ„“ÖŃĪĖ®ÖŠµÄ![]() ŗĶ
ŗĶ![]() £¬ŠčŅŖ¼ÓČėµÄŹŌ¼Į·Ö±šĪŖ_______”¢___________”£
£¬ŠčŅŖ¼ÓČėµÄŹŌ¼Į·Ö±šĪŖ_______”¢___________”£
¢Śµē½ā¹ż³ĢÖŠ±»Ńõ»ÆµÄĪļÖŹŹĒ________”£
¢ŪæÉÓĆ![]() ČÜŅŗĪüŹÕµē½ā²śÉśµÄ
ČÜŅŗĪüŹÕµē½ā²śÉśµÄ![]() £¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ______________”£
£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ______________”£
(4)²Ł×÷III£ŗ
ĀĖŅŗ»ńĄūNaClO2µÄ²Ł×÷²½Öč£ŗ¢Ł¼ÓČČÕō·¢£»¢Ś³ĆČČ¹żĀĖ£»¢ŪĻ“µÓ£»¢ÜøÉŌļ£¬µĆµ½³ÉĘ·”£³ĆČČ¹żĀĖÓ¦æŲÖʵÄĪĀ¶Č·¶Ī§ŹĒ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒė½«·ūŗĻĢāŅāµÄĻĀĮŠ±ä»ÆµÄŠņŗÅĢīŌŚ¶ŌÓ¦µÄŗįĻßÉĻ£ŗ¢ŁµāµÄÉż»Ŗ£»¢ŚŃõĘųČÜÓŚĖ®£»¢ŪĀČ»ÆÄĘČÜÓŚĖ®£»¢ÜÉÕ¼īČŪ»Æ£»¢ŻĀČ»ÆĒāČÜÓŚĖ®£»¢ŽĀČ»Æļ§ŹÜČČ·Ö½ā”£
(1)»Æѧ¼üƻӊ±»ĘĘ»µµÄŹĒ__________£»½ö·¢ÉśĄė×Ó¼üĘĘ»µµÄŹĒ__________£»
(2)¼“·¢ÉśĄė×Ó¼üĘĘ»µ”¢ÓÖ·¢Éś¹²¼Ū¼üĘĘ»µµÄŹĒ____________________£»
(3)N2µÄµē×ÓŹ½ĪŖ__________£»Na2O2µÄµē×ÓŹ½ĪŖ___________£»CO2µÄµē×ÓŹ½ĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æC1O2ŹĒŅ»ÖÖĻū¶¾É±¾śŠ§ĀŹøß”¢¶ž“ĪĪŪČ¾Š”µÄĖ®“¦Ąķ¼Į”£ŹµŃéŹŅæÉĶعżŅŌĻĀ·“Ó¦ÖʵĆC1O2£ŗ2KClO3+H2C2O4+H2SO4![]() 2ClO2”ü+K2SO4+2CO2”ü+2H2O,ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
2ClO2”ü+K2SO4+2CO2”ü+2H2O,ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A. ŌŚ·“Ó¦ÖŠH2C2O4¼Č²»ŹĒŃõ»Æ¼ĮŅ²²»ŹĒ»¹Ō¼Į
B. 1 mol KClO3²Ī¼Ó·“Ó¦£¬ŌŚ±ź×¼×“æöĻĀÄܵƵ½22.4 LĘųĢå
C. 1 mol KClO3²Ī¼Ó·“Ó¦ÓŠ2 molµē×Ó×ŖŅĘ
D. KClO3ŌŚ·“Ó¦ÖŠŹĒŃõ»Æ¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌŠæĆĢ·Ļµē³ŲÖŠµÄĢ¼°ü£Øŗ¬Ģ¼·Ū”¢Fe”¢Cu”¢AgŗĶMnO2µČĪļÖŹ £©ĪŖŌĮĻ»ŲŹÕMnO2µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
I.½«Ģ¼°üÖŠĪļÖŹŗęøÉ£¬ÓĆ×ćĮæĻ”HNO3Čܽā½šŹōµ„ÖŹ£¬¹żĀĖ£¬µĆĀĖŌüa£»
II.½«ĀĖŌüaŌŚæÕĘųÖŠ×ĘÉÕ³żČ„Ģ¼·Ū£¬µĆµ½“ÖMnO2£»
III.Ļņ“ÖMnO2ÖŠ¼ÓČėĖįŠŌH2O2ČÜŅŗ£¬MnO2ČܽāÉś³ÉMn2+£¬ÓŠĘųĢåÉś³É£»
IV. ĻņIIIĖłµĆČÜŅŗ£ØpHŌ¼ĪŖ6£©ÖŠ»ŗĀżµĪ¼Ó0.50 molL-1 Na2CO3ČÜŅŗ£¬¹żĀĖ£¬µĆĀĖŌüb£¬ĘäÖ÷ŅŖ³É·ÖĪŖMnCO3£»
V. ĀĖŌüb¾Ļ“µÓ”¢øÉŌļ”¢×ĘÉÕ£¬ÖĘµĆ½Ļ“æµÄMnO2”£
£Ø1£©¦©ÖŠAgÓė×ćĮæĻ”HNO3·“Ӧɜ³ÉNOµÄ»Æѧ·½³ĢŹ½ĪŖ____________________”£
£Ø2£©ŅŃÖŖIIµÄ×ĘÉÕ¹ż³ĢÖŠĶ¬Ź±·¢Éś·“Ó¦£ŗ
MnO2(s)+C(s) = MnO(s) + CO (g) ”÷H=+24.4 kJ mol -1
MnO2(s)+CO(g) = MnO(s)+CO2(g) ”÷H=-148.1 kJ mol -1
Š“³öMnO2ŗĶC·“Ӧɜ³ÉMnOŗĶCO2µÄČČ»Æѧ·½³ĢŹ½£ŗ________”£
£Ø3£©H2O2·Ö×ÓÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶĪŖ________”¢________”£
£Ø4£©IIIÖŠMnO2ČܽāµÄĄė×Ó·½³ĢŹ½ĪŖ________£¬ČܽāŅ»¶ØĮæµÄMnO2£¬H2O2µÄŹµ¼ŹĻūŗÄĮæ±ČĄķĀŪÖµøߣ¬ÓĆ»Æѧ·½³ĢŹ½½āŹĶŌŅņ£ŗ______________________________________”£
£Ø5£©IVÖŠ£¬ČōøÄĪŖ”°Ļņ0.50 molL-1 Na2CO3ČÜŅŗÖŠ»ŗĀżµĪ¼ÓIIIĖłµĆČÜŅŗ”±£¬ĀĖŌübÖŠ»į»ģÓŠ½Ļ¶ąMn(OH)2³Įµķ£¬½āŹĶĘäŌŅņ£ŗ________________________________________”£
£Ø6£©VÖŠMnCO3ŌŚæÕĘųÖŠ×ĘÉյĻÆѧ·½³ĢŹ½ĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚøŹ°±Ėį£ØH2N-CH2-COOH£©ŠŌÖŹµÄĖµ·ØÖŠÕżČ·µÄŹĒ
A. Ö»ÓŠĖįŠŌ£¬Ć»ÓŠ¼īŠŌB. Ö»ÓŠ¼īŠŌ£¬Ć»ÓŠĖįŠŌ
C. ¼ČÓŠĖįŠŌ£¬ÓÖÓŠ¼īŠŌD. ¼ČƻӊĖįŠŌ£¬ÓÖƻӊ¼īŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņijĆܱÕČŻĘ÷ÖŠ³äČė1 mol XÓė2 mol Y·¢Éś·“Ó¦£ŗX(g)£«2Y(g) ![]() aZ(g)””¦¤H£¼0£¬“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ģõ¼ž(ĪĀ¶Č»ņČŻĘ÷Ģå»ż)£¬XµÄĘ½ŗā×Ŗ»ÆĀŹµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
aZ(g)””¦¤H£¼0£¬“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ģõ¼ž(ĪĀ¶Č»ņČŻĘ÷Ģå»ż)£¬XµÄĘ½ŗā×Ŗ»ÆĀŹµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)

A. a =2 B. T2£¾T1
C. AµćµÄ·“Ó¦ĖŁĀŹ£ŗvÕż(X)=![]() vÄę(Z) D. ÓĆY±ķŹ¾A”¢BĮ½µćµÄ·“Ó¦ĖŁĀŹ£ŗv(A)£¾v(B)
vÄę(Z) D. ÓĆY±ķŹ¾A”¢BĮ½µćµÄ·“Ó¦ĖŁĀŹ£ŗv(A)£¾v(B)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæĪŖ31µÄCOŗĶO2×é³ÉµÄ»ģŗĻĘųĢå4mol£¬³ä·ÖČ¼ÉÕŗ󣬽«²śÉśµÄĘųĢåĮ¢¼“ĶØČėµ½×ćĮæNa2O2¹ĢĢåÖŠ£¬Na2O2¹ĢĢåŌö¼ÓµÄÖŹĮæŹĒ£Ø £©
A. 28 g B. 32 g
C. 31 g D. ĪŽ·Ø¼ĘĖć
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com