


 分子式:
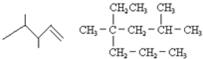
分子式: 的结构简式为(CH3)2CHCH2CH2CH3;
的结构简式为(CH3)2CHCH2CH2CH3; 的结构简式为CH2=CHCH3CH2CH3;
的结构简式为CH2=CHCH3CH2CH3; ;
; ;
; ;
; ;
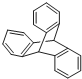
; 分子式为C20H14,分子中含有3个苯环,不属于苯的同系物;
分子式为C20H14,分子中含有3个苯环,不属于苯的同系物;

科目:高中化学 来源: 题型:
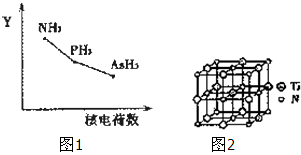 我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖.
我国化学家在“铁基(氟掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,该研究项目荣获2013年度“国家自然科学奖”一等奖.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol?L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
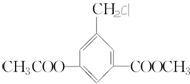 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )| A、该物质能发生消去反应 |
| B、苯环上的一氯代物有2种 |
| C、含有一种含氧官能团 |
| D、分子式是C10H12O4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去NaCl固体中少量的NH4Cl,可用加热的方法除去 |
| B、除去NO2气体中少量的NO气体,可通入适量的O2 |
| C、除去FeSO4溶液中少量的Fe2(SO4)3,可加入Cu粉充分反应后过滤 |
| D、除去NaHCO3固体中少量的Na2CO3,可用加热至恒重的方法除去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com