
下列有关离子反应或离子方程式的叙述中,正确的是( )
A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存
B.惰性电极电解氯化铝溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.镁与极稀硝酸反应生成硝酸铵的离子方程式为4Mg+6H++NO3—=4Mg2++NH4++3H2O
D.将10 mL 0.1 mol·L-1 KAl(SO4)2溶液和10 mL 0.2 mol·L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1∶2
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题8电解质溶液练习卷B(解析版) 题型:选择题
常温时,下列叙述正确的是( )
A.稀释pH=10的氨水,溶液中所有离子的浓度均降低
B.pH均为5的HCl和NH4Cl溶液中,水的电离程度相同
C.NaOH和CH3COONa的混合溶液中,c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题6物质结构与元素周期律练习卷(解析版) 题型:选择题
下表是元素周期表的一部分,有关说法正确的是( )

A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.6种元素中,c元素单质的化学性质最活泼
D. c、e、f的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题5化学反应中的能量变化练习卷(解析版) 题型:选择题
已知:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol;②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。下列结论正确的是( )
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题4离子反应练习卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.向碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca2++2HCO3—+2OH-=CaCO3↓+CO32—+2H2O
B.向偏铝酸钠溶液中通入过量二氧化碳气体:AlO2—+CO2+2H2O=Al(OH)3↓+HCO3—
C.以石墨作电极电解氯化铝溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.漂白粉溶液中通入足量二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3—
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题4离子反应练习卷(解析版) 题型:选择题
一包白色粉末,由几种常见的盐混合组成,其中只可能含有Na+、K+、Al3+、CO32—、HCO3—、SO42—、SO32—、NO3—中的若干种离子。某同学对该溶液进行如下实验:
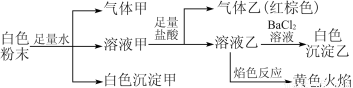
以下说法正确的是( )
A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和HCO3—
B.气体乙一定是NO和NO2的混合气体
C.白色沉淀乙是BaSO4,所以原混合物一定含有SO42—
D.焰色反应为黄色火焰,不能确定原混合物中不含K+
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题17有机化学基础练习卷(解析版) 题型:填空题
醛类是有机合成中的重要原料,特别是对有机物碳链增长起着重要的桥梁作用。
如醛类在一定条件下有如下反应:
CH3CHO+Br—CH—COOC2H5CH3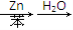 CH3—CH—CH—COOC2H5OHCH3
CH3—CH—CH—COOC2H5OHCH3
用CH3—CH—COOHOH通过以下路线可合成(G):
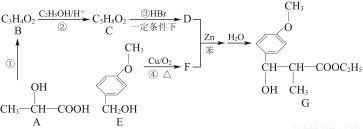
(1)反应①的条件是 。
(2)B的结构简式为 ,其核磁共振氢谱显示分子内有3种不同环境的氢原子,其个数比为 。
(3)反应②和④的类型是 、 。
(4)D与足量的热NaOH溶液反应的化学方程式为 。
(5)F的一种同分异构体能发生银镜反应,还能水解生成不含甲基的芳香化合物W,W的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题15化学与技术练习卷(解析版) 题型:填空题
由铝土矿(主要成分是Al2O3)炼制铝的工艺流程示意图如下:
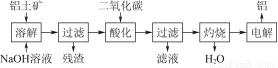
(1)电解生成的铝在熔融液的 (填“上层”或“下层”),电解时不断消耗的电极是 (填“阴极”或“阳极”)。
(2)写出通入过量二氧化碳酸化时反应的离子方程式
。
(3)电解制备铝时,需加入冰晶石(Na3AlF6),其作用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式 。
(4)上述工艺所得铝中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池的阴极材料是 (填化学式),阳极的电极反应式为 。
(5)对金属制品进行抗腐蚀处理,可延长其使用寿命。
①控制一定条件进行电解(见图),此时铝表面可形成耐酸的致密氧化膜,其电极反应式为 ;
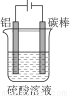
②钢材镀铝后,能防止钢材腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题12有机物的结构与性质练习卷(解析版) 题型:选择题
维生素C是人体维持正常生命过程所必需的一种物质,主要来源于新鲜的蔬菜和水果中,其结构如图所示。下列关于维生素C的说法中正确的是( )
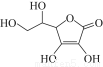
A.属于有机物,难溶于水,易溶于有机溶剂
B.能使FeCl3溶液显紫色
C.能使溴的四氯化碳溶液褪色
D.在一定条件下,能发生加成反应和氧化反应,但不能发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com