
����Ŀ��һ������������������ȼ�գ����û������100ml 3.0mol/L��NaOH��Һǡ����ȫ���գ������Һ�к���NaClO�����ʵ���Ϊ0.05mol��
(1)д��ʵ�����������Ļ�ѧ����ʽ_______________________________���������뻹ԭ�������ʵ���֮��Ϊ ________��
(2)����������������Һ��Ӧ�����ӷ���ʽΪ _______________________________ ��
(3)������Һ��Cl-�����ʵ���Ϊ_____________mol��
(4)ԭ����������������������ʵ���֮��Ϊ_____________��
���𰸡�MnO2 +4HCl(Ũ) ![]() MnCl2 +Cl2��+2H2O 1��2 Cl2+2OH-=Cl-+ClO-+H2O 0.25 3��2
MnCl2 +Cl2��+2H2O 1��2 Cl2+2OH-=Cl-+ClO-+H2O 0.25 3��2
��������
ʵ��������MnO2��Ũ������ȡCl2��Cl2��NaOH ��Һ��Ӧ����NaCl��NaClO���������֪������������Ӧ������ΪHCl��Cl2���漰��Ӧ��HCl+NaOH=NaCl+H2O��Cl2+2NaOH=NaCl+NaClO+H2O�����������غ���㡣
��1��ʵ��������MnO2��Ũ������ȡCl2���仯ѧ����ʽ��MnO2 +4HCl(Ũ) ![]() MnCl2 +Cl2��+2H2O��������ΪMnO2����ԭ��ΪHCl�������ʵ���֮��Ϊ��1��2���ʴ�Ϊ��MnO2 +4HCl(Ũ)
MnCl2 +Cl2��+2H2O��������ΪMnO2����ԭ��ΪHCl�������ʵ���֮��Ϊ��1��2���ʴ�Ϊ��MnO2 +4HCl(Ũ) ![]() MnCl2 +Cl2��+2H2O��1��2��
MnCl2 +Cl2��+2H2O��1��2��
��2��Cl2��NaOH ��Һ��Ӧ����NaCl��NaClO�������ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��3��������Һ��ΪNaCl��NaClO�Ļ���������ݵ���غ�n(Na+)=n(Cl-)+n(ClO-)����n(Cl-)=n(Na+)-n(ClO-)=0.3mol-0.05mol=0.25mol���ʴ�Ϊ��0.25��
��4���������֪������������Ӧ�����û����ΪHCl��Cl2���漰��Ӧ��HCl+NaOH=NaCl+H2O��Cl2+2NaOH=NaCl+NaClO+H2O���ݷ�Ӧ��֪��ȼ�պ�ʣ��Cl2Ϊn(Cl2)��=n(NaClO)=0.05 mol����H2��Ӧ��Cl2Ϊn(Cl2)=![]() ��[n(Cl-)-n(NaClO)]=
��[n(Cl-)-n(NaClO)]=![]() ��(0.25mol-0.05mol)=0.1mol=n(H2)����ԭ����������������������ʵ���֮��
��(0.25mol-0.05mol)=0.1mol=n(H2)����ԭ����������������������ʵ���֮��
n(Cl2)��n(H2)=(0.1mol+0.05mol)��0.1mol=3��2���ʴ�Ϊ��3��2��


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����£����ԣ�HF>HCN���ֱ���1L1mol/L��HF��HCN��Һ�м�NaOH�������pH�������¶Ⱥ���Һ����ı仯������Һ�еģ�X��ʾF��CN����pH�仯��ͼ��ʾ������˵����ȷ����
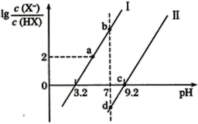
A.HF�ĵ��볣��Ka(HF)��������10-4
B.d����Һ�У�c(Na+)=c(X-)>c(HX)
C.a��b��Ĺ�����ˮ�ĵ���̶��ȱ����С
D.b����Һ��d����Һ��c(Na+)��b<d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӽ���������ˮ������ͼ��ʾ������˵���д������

A. ���������ӽ�����֬��ˮ�������ӵ���������
B. ˮ�е�![]() ��
��![]() ��Clͨ����������֬��ȥ
��Clͨ����������֬��ȥ
C. ͨ������������ˮ�ĵ����Խ���
D. ��������֬���δ��ڷ�ӦH++OH![]() H2O
H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ NO2+NH3��N2+H2O��δ��ƽ����������װ��ͼ��ʾ�ĵ�أ��������������������Ⱦ�������йظõ��˵��һ����ȷ���� �� ��

A.�缫��Ϊ��ظ���
B.���ӽ���ĤΪ���ӽ���Ĥ
C.������ӦʽΪ 2NH3-6e-+6OH-=N2��+6H2O
D.28.0L����״����NO2 ��ȫ��������ת�� 4mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����
A.1mol ������ˮ������ȫ��Ӧת�Ƶĵ�����Ϊ2NA
B.���³�ѹ�£�1mol �������е�ԭ����ΪNA
C.��״���£�11. 2 L �Ҵ����еķ�����ĿΪ0. 5NA
D.���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl- ����Ϊ NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2A(g)![]() 2B(g)+C(g)�ں�ѹ���ܱ������з�Ӧ������ѡ���в���˵����Ӧ�Ѵﵽƽ��״̬����( )
2B(g)+C(g)�ں�ѹ���ܱ������з�Ӧ������ѡ���в���˵����Ӧ�Ѵﵽƽ��״̬����( )
A. �����������ܶȲ��ٸı��״̬
B. v(A):v(B):v(C)=2:2:1
C. c(A):c(B):c(C)��ֵ���ֲ���
D. ��������ƽ����Է����������ٸı��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������У���Ϊͬλ�ص��� __________ ����Ϊͬ����������� ________ ����Ϊͬϵ�����______________ ����Ϊͬ���칹�����_____________
�ٽ��ʯ��ʯī ��12C��14C ��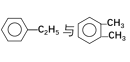 ��
��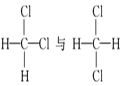 ��
�� ��
��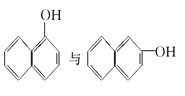 ��CH4��C(CH3)4
��CH4��C(CH3)4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ƿ�������ʱ���õ����������Խ��еĻ�����������ֱ��ǣ���
![]()
A.�����ˡ���ȡ������B.������������ȡ������
C.��ȡ�����ˡ���������D.���ˡ���������ȡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ��ȤС���Ʊ�����Һ����Ҫ�ɷ���NaClO�������������װ�á�
��֪��Cl2��NaOH��Һ�ܷ������з�Ӧ
�ڼ���ʱ��![]()
�ڵ���ʱ��![]()
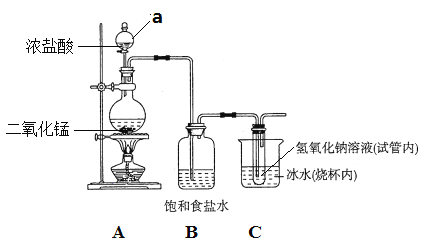
�Իش��������⣺
������a��������_____________��
�����Ӻ�װ�ã�װҩƷ֮ǰ��������е�һ�������_________________��
��Aװ���ڷ�����Ӧ�Ļ�ѧ����ʽΪ_______________________________��
��B��������___________����ˮ��������__________________________��
�ɸ�װ�õIJ���֮����___________________________________________��
��һ���¶��£���NaOH��Һ��ͨ��һ����������������ǡ����ȫ��Ӧ���������к������ֺ���Ԫ�ص����ӣ�����ClO����ClO3���������ӵ����ʵ�����n���뷴Ӧʱ�䣨t����������ͼ��ʾ��
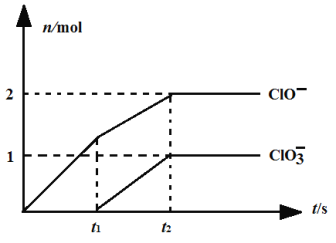
�ù�����t2ʱ�̲μӷ�Ӧ��Cl2���ʵ���Ϊ_________mol������һ���̲�����n(Cl��)Ϊ5.5mol��n(ClO3��)Ϊ1mol����μӷ�Ӧ��NaOH���ʵ���Ϊ___________________mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com