
【题目】向足量的500 mL NaOH溶液中投入10.8 g Al,二者恰好完全反应。试计算:
(1)Al的物质的量。
(2)参加反应的NaOH的物质的量和溶液的物质的量浓度。
(3)生成标准状况下H2的体积。
【答案】(1)0.4 mol(2分)
(2)0.8 mol/L(4分)
(3)13.44 L(3分)
【解析】根据物质的量、摩尔质量和质量之间的等式关系,n=![]() ,能求出Al的物质的量。由反应的化学方程式能求出参加反应的NaOH和生成H2的物质的量,则能求出NaOH溶液的物质的量浓度及标准状况下H2的体积。
,能求出Al的物质的量。由反应的化学方程式能求出参加反应的NaOH和生成H2的物质的量,则能求出NaOH溶液的物质的量浓度及标准状况下H2的体积。
(1)n(Al)=![]() =0.4 mol。
=0.4 mol。
(2)设参加反应的NaOH物质的量是n。
2Al + 2NaOH+2H2O===2NaAlO2+3H2↑
2 mol 2 mol
0.4 mol n
则![]() ,n=0.4 mol,c(NaOH)=
,n=0.4 mol,c(NaOH)=![]() =0.8 mol/L。
=0.8 mol/L。
(3)设生成标准状况下H2的体积是V。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
2 mol 3×22.4 L
0.4 mol V
V=![]() =13.44 L。
=13.44 L。


科目:高中化学 来源: 题型:
【题目】Ⅰ.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X、Y既不同族,也不同周期。X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价
的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)请写出M的元素符号:____________,Z的原子结构示意图:_____________。M与X两元素可形成两种液态化合物,其化学式分别为________________________。
(2)请写出N元素在周期表中的位置:___________________________;与N同族的短周期元素L,其最高价氧化物的电子式为_______________________。
(3)Y与Z相比,非金属性较强的元素是__________(填元素符号),可以证明该结论的实验事实是_________________________________________________________________。
Ⅱ.下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。
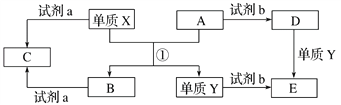
(1)请写出反应①的化学方程式:_____________________________________。
(2)由D到E的离子方程式:__________________。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:__________________________________________________________________。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将淀粉与氯化钾混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是( )
A. 加入碘水变蓝色
B. 加入硝酸银溶液不产生白色沉淀
C. 加入硝酸银溶液产生白色沉淀
D. 加入碘水不变色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国晋代《抱朴子》中描述了大量的化学反应,其中有:①“丹砂(HgS)烧之成水银,积变又还成丹砂”; ②“以曾青涂铁,铁赤色如铜”。下列有关叙述正确的是
A. ①中水银“积变又还成丹砂”说明水银发生了还原反应
B. ②中反应的离子方程式为:2Fe+3Cu2+=2Fe3++3Cu
C. 根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒
D. 水银能跟曾青发生置换反应生成单质铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式中,错误的是( )
A. 将氨通入盐酸中:NH3+H+===NH4+
B. 在NaOH溶液中滴入NH4Cl溶液:NH4++OH-===NH3.H2O
C. 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-===Cu2++2NO2 ↑+2H2O
D. 将稀硫酸滴在铜片上:Cu+2H+===Cu2++H2 ↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol铜与40 mL 10 mol/L HNO3充分反应后,溶液中含a mol H+。由此可知
A.生成的气体在标准状况下的体积为4.48 L
B.生成的气体在标准状况下的体积为1.49 L
C.被还原的硝酸的物质的量为(0.2a)mol
D.反应后溶液中所含![]() 的物质的量为0.2 mol
的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁二酮肟(![]() )是检验Ni2+的灵敏试剂。
)是检验Ni2+的灵敏试剂。
(1)Ni2+基态核外电子排布式为________。丁二酮肟分子中C原子轨道杂化类型为________,1 mol丁二酮肟分子所含σ键的数目为________,分子中各原子的电负性由大到小的顺序为________________。
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点-19.3 ℃,沸点42.1 ℃,易溶于有机溶剂。
①Ni(CO)4固态时属于________晶体(填晶体类型)。
②与CO互为等电子体的阴离子为____________(填化学式)。
(3)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________________________。
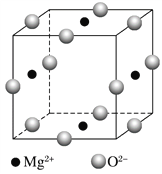
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com