
| A. | NaOH | B. | CH3COOH | C. | BaSO4 | D. | CH3COONa |
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=10-13mol•L-1的溶液中:Na+、NH4+、Cl-、NO3- | |
| B. | 1.0 mol•L-1KI溶液中:Mg2+、Fe2+、SO42-、ClO- | |
| C. | c(Fe3+)=0.1 mol•L-1的溶液中:Na+、NH4+、HCO3-、I- | |
| D. | 饱和氨水中:NH4+、Ag+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 位置 | A与B相差质子数 | 离子半径比较 | ||||
| 周期 | 主族 | 纵行 | ||||
| Am+与Bn-相差两个电子层 | A | |||||
| B | ||||||
| Am+与Bn-相差一个电子层 | A | |||||
| B | ||||||
| Am+与Bn-电子层结构相同 | A | |||||
| B | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量NH4Cl固体,平衡逆移溶液中c(NH4+)减小 | |
| B. | 加入少量浓盐酸,浓盐酸与 NH3•H2O反应,电离平衡逆移 | |
| C. | 加热,电离平衡逆移 | |
| D. | 加水后,溶液中n(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
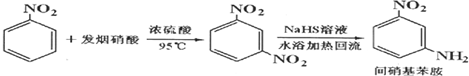
| 参考数据 | 组分 | 邻硝基苯胺 | 间硝基苯胺 | 对硝基苯胺 | 水 | 甲醇 | 硝基苯 |
| 沸点/℃ | 284 | 305.7 | 331.7 | 100 | 64.7 | 4.75 | |
| 偶极矩/D | 4.38 | 4.91 | 6.33 | 1.85 | 1.69 | 4.75 | |
| 颜色 | 橙色 | 淡黄色 | 淡黄色 | 无色 | 无色 | 淡黄色 |

 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com