
| A. | 铝盐和铁盐具有净水的作用 | |
| B. | 小苏打是治疗胃酸过多的一种药剂 | |
| C. | 硅胶可防止月饼等富脂食品因被氧化而变质 | |
| D. | 青铜是我国使用最早的合金材料 |
分析 A.铝盐、铁盐均可水解生成胶体,具有吸附性;
B.小苏打为碳酸氢钠,能够与盐酸反应;
C.防止月饼等富脂食品因被氧化而变质应加入还原性物质;
D.铜合金为最早使用的金属材料.
解答 解:A.铝盐、铁盐均可水解生成胶体,具有吸附性,吸附水中悬浮杂质可净化水,故A正确;
B.小苏打为碳酸氢钠,能够与盐酸反应,消耗盐酸,且碳酸氢钠碱性较弱,所以可以用于治疗胃酸过多,故B正确;
C.硅胶不具有还原性,不能防止月饼等富脂食品因被氧化而变质,具有吸水性,可以防止食物受潮变质,故C错误;
D.青铜是我国使用最早的合金材料,故D正确;
故选C.
点评 本题考查了化学与生活、生产关系,侧重考查物质的用途,性质决定用途,明确相关物质的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铁粉溶于稀盐酸:2Fe+6H+═2Fe3++3H2 | |
| B. | 碳酸钙溶于稀盐酸中:CO32-+2H+═CO2+H2O | |
| C. | 氧化铜溶于醋酸:CuO+2CH3COOH═Cu2++2CH3COO-+H2O | |
| D. | 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-═BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
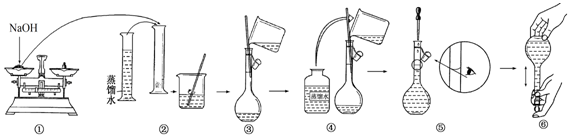
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

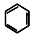 +CH2=CH2$\stackrel{H_{2}SO_{4}}{→}$
+CH2=CH2$\stackrel{H_{2}SO_{4}}{→}$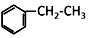
 .
. .
.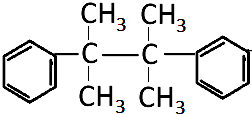 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠与水反应:2O22-+2H2O═4OH-+O2↑ | |
| B. | 氧化铝与盐酸:O2-+2H+═H2O | |
| C. | NaOH溶液与小苏打溶液反应:HCO3-+OH-═CO32-+H2O | |
| D. | 氯气通入水中:Cl2+H2O?2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应在一定条件下可自发进行,放热反应在任何条件下都可以自发进行 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使化学反应速率增大主要原因是增加了反应物分子中活化分子的百分数 | |
| D. | 升高温度或加入催化剂,可以改变化学反应的反应热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com